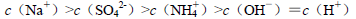在密闭容器中充入一定量的NO2,发生反应2NO2(g) N2O4(g) △H=-57kJ/mol,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化的曲线如下图所示。下列说法正确的是
N2O4(g) △H=-57kJ/mol,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化的曲线如下图所示。下列说法正确的是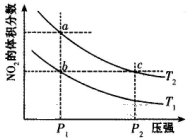
| A.a、c两点的反应速率:a>c |
| B.a、b两点的转化率:a<b |
| C.a、c两点气体的颜色:a深,c浅 |
| D.由a点到b点,可以用加热的方法 |
T℃时在2 L密闭容器中使X(g)与Y(g)发生反应生成Z(g)。反应过程中X、Y、Z的浓度变化如图1所示;若保持其他条件不变,温度分别为T1和T2时,Y的体积分数与时间的关系如图2所示。则下列结论正确的是 
A.反应进行的前3 min内,用X表示的反应速率 |
| B.平衡时容器内的压强为反应前的0.9倍 |
| C.保持其他条件不变,升高温度,反应的化学平衡常数K减小 |
| D.若改变反应条件,使反应进程如图3所示,则改变的条件是增大压强 |
对处于平衡状态的反应2A(g)+B(g) 2C(g) △H<0,下列叙述正确的是
2C(g) △H<0,下列叙述正确的是
| A.增大A浓度的瞬间,V正 增大,V逆不变 |
| B.升高温度,V正 减小,V逆增大 |
| C.增大压强. V正 增大,V逆 减小 |
| D.加入催化剂,V正、V逆 都增大 |
反应2X(g)+Y(s) 2Z(g) ΔH<0,达到平衡时,下列说法正确的是
2Z(g) ΔH<0,达到平衡时,下列说法正确的是
| A.减小容器体积,平衡不移动 |
| B.增大Y的量,Z的百分含量增大 |
| C.加入催化剂,X的转化率增大 |
| D.降低温度,正反应速率增大、逆反应速率减小 |
对于可逆反应N2(g)+3H2(g) 2NH3(g) ΔH<0,下列研究目的和示意图相符的是( )。
2NH3(g) ΔH<0,下列研究目的和示意图相符的是( )。
| | A | B |
| 研究 目的 | 压强对反应的影 响(p2>p1) | 温度对反应的影响 |
| 图示 | 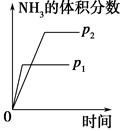 | 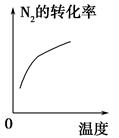 |
| 研究 目的 | 平衡体系增加N2 对反应的影响 | 催化剂对反应的影响 |
| 图示 |  | 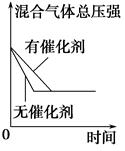 |
在一密闭容器中,放入镍粉并充入一定量的CO气体,一定条件下发生反应:Ni(s)+4CO(g) Ni(CO)4(g),已知该反应在25 ℃和80 ℃时的平衡常数分别为5×104、2,下列说法正确的是( )。
Ni(CO)4(g),已知该反应在25 ℃和80 ℃时的平衡常数分别为5×104、2,下列说法正确的是( )。
| A.上述生成Ni(CO)4(g)的反应为吸热反应 |
| B.在80 ℃时,测得某时刻Ni(CO)4、CO浓度均为0.5 mol·L-1,则此时v(正)<v(逆) |
| C.恒温恒压下,向容器中再充入少量的Ar,上述平衡将正向移动 |
| D.恒温恒容下,向容器中再充入少量Ni(CO)4(g),达新平衡时,Ni(CO)4的百分含量将增大 |
一定温度下,容积为2 L的甲、乙两固定容积的密闭容器中,发生反应:2SO2(g)+O2(g)  2SO3(g)。达平衡时测得有关数据如下表。
2SO3(g)。达平衡时测得有关数据如下表。
| 容器 | 甲 | 乙 |
| 反应物投入量 | 2 mol SO2、1 mol O2 | 4 mol SO3 |
| n(SO3)/mol | 1.6 | a |
| 反应物的转化率 | α1 | α2 |
下列说法正确的是( )。
A.α1+α2>1
B.1.6<a<3.2
C.若甲中反应2 min时达到平衡,则2 min 内平均速率v(O2)=0.2 mol·L-1·min-1
D.甲平衡后再加入0.2 mol SO2、0.2 mol O2和0.4 mol SO3,平衡正向移动
下列有关说法正确的是( )。
| A.NH4Cl(s)=NH3(g)+HCl(g)室温下不能自发进行,说明该反应的ΔH<0 |
| B.镀锌铁制品镀层破损后,铁制品比受损前更容易生锈,而镀锡铁则相反 |
C.对于N2(g)+3H2(g) 2NH3(g),当其他条件不变时,压缩气体体积使压强增大,正反应和逆反应速率以及H2的平衡转化率均增大 2NH3(g),当其他条件不变时,压缩气体体积使压强增大,正反应和逆反应速率以及H2的平衡转化率均增大 |
| D.100 ℃时水的离子积常数KW为5.5×10-13,说明水的电离是放热反应 |
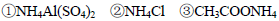
 由大到小的顺序是
由大到小的顺序是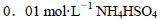 溶液中滴加NaOH溶液至中性:
溶液中滴加NaOH溶液至中性: