在密闭容器中,一定条件下进行如下反应NO(g)+CO(g)
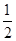 N2(g)+CO2(g),ΔH=-373.2 kJ/mol,达到平衡后,为提高该反应的速率和NO的转化率,采取的正确措施是( )
N2(g)+CO2(g),ΔH=-373.2 kJ/mol,达到平衡后,为提高该反应的速率和NO的转化率,采取的正确措施是( )
| A.加催化剂同时升高温度 | B.加催化剂同时增大压强 |
| C.升高温度同时充入N2 | D.降低温度同时增大压强 |
已知4NH3(g)+5O2(g) 4NO(g)+6H2O(g),若化学反应速率分别用v(NH3)、v(O2)、v(NO)、v(H2O)[单位:mol/(L·s)]表示,则正确关系是( )
4NO(g)+6H2O(g),若化学反应速率分别用v(NH3)、v(O2)、v(NO)、v(H2O)[单位:mol/(L·s)]表示,则正确关系是( )
A.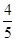 v(NH3)=v(O2) v(NH3)=v(O2) | B.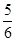 v(O2)=v(H2O) v(O2)=v(H2O) |
C.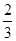 v(NH3)=v(H2O) v(NH3)=v(H2O) | D.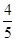 v(O2)=v(NO) v(O2)=v(NO) |
升高温度时,化学反应速率加快,主要原因是( )
| A.分子运动速率加快,使该反应物分子的碰撞机会增多 |
| B.反应物分子的能量增加,活化分子百分数增大,有效碰撞次数增多 |
| C.该化学反应的过程是吸热的 |
| D.该化学反应的过程是放热的 |
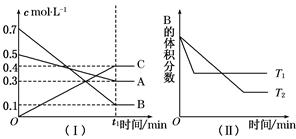
一定条件下,使X(g)与Y(g)在2L密闭容器中发生反应生成z(g)。温度为TK时,反应过程中X,Y,Z的物质的量变化如图1所示;若保持其他条件不变,温度分别为T, K和T2 K时,Y的体积分数与时间的关系如图2所示。则下列结论正确的是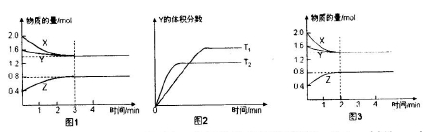
| A.反应进行的前3 min内,用X表示的反应速率V(X)=0.1 mol/(L·min) |
B.平衡时容器内的压强为反应前的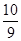 倍 倍 |
| C.保持其他条件不变,升高温度,反应的化学平衡常数K减小 |
| D.若改变反应条件,使反应进程如图3所示,则改变的条件是增大压强 |
对于可逆反应N2(g)+3H2(g) 2NH3(g)(正反应为放热反应),下列说法中正确的是( )
2NH3(g)(正反应为放热反应),下列说法中正确的是( )
| A.达到平衡后加入N2,当重新达到平衡时,NH3的浓度比原平衡的大,N2的浓度比原平衡的小 |
| B.达到平衡后,升高温度,既加快了正、逆反应速率,又提高了NH3的产率 |
| C.达到平衡后,缩小容器体积,既有利于加快正、逆反应速率,又有利用提高氢气的转化率 |
| D.加入催化剂可以缩短达到平衡的时间,是因为正反应速率增大了,而逆反应速率减小了 |
合成氨反应的正反应是气体体积减小的放热反应。合成氨工业的生产流程如下: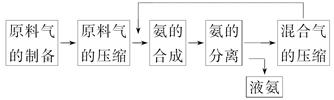
关于合成氨工业的说法中不正确的是( )
| A.混合气进行循环利用遵循绿色化学思想 |
| B.合成氨反应须在低温下进行 |
| C.对原料气进行压缩是为了增大原料气的转化率 |
| D.使用催化剂可以提高反应的速率,但是不能使平衡向正反应方向移动 |
已知200 ℃,反应2NO(g)+2CO(g) 2CO2(g)+N2(g)的平衡常数K=10,则下列情况达到平衡状态的是( )
2CO2(g)+N2(g)的平衡常数K=10,则下列情况达到平衡状态的是( )
| | c(NO) | c(CO) | c(CO2) | c(N2) |
| A | 1 | 1 | 0.1 | 0.1 |
| B | 0.1 | 0.1 | 0.1 | 0.1 |
| C | 0.2 | 0.1 | 0.2 | 1 |
| D | 0.3 | 0.2 | 0.2 | 0.3 |
下列反应在任意温度下一定能自发进行的是( )
A.2NaCl+2H2O 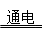 2NaOH+Cl2↑+H2↑ 2NaOH+Cl2↑+H2↑ |
| B.NH3(g)+HCl(g)=NH4Cl(s) ΔH<0 |
| C.CaCO3(s)=CaO(s)+CO2(g) ΔH>0 |
| D.X2Y2(g)=X2(g)+Y2(g) ΔH<0 |
 A. B. C. D.
A. B. C. D.