题目内容
在相同条件下,取等量H2O2做H2O2分解的对比实验,其中(1)加入MnO2催化,(2)不加MnO2催化。下图是反应放出O2的体积随时间的变化关系示意图,其中正确的是( ) A. B. C. D.
A. B. C. D.
A
解析
试题分析:催化剂能加快化学反应速率,使等质量的H2O2首先达到产生气体的最大值,但是不能改变产生氧气的体积的多少。因此正确选项为A。

练习册系列答案
相关题目
相同温度下,体积均为1.5 L的两个恒容容器中发生可逆反应:
X2 (g+3Y2(g)  2XY3(g) ΔH=-92.6 kJ·mol-1,实验测得有关数据如下表:
2XY3(g) ΔH=-92.6 kJ·mol-1,实验测得有关数据如下表:
| 容器编号 | 起始时各物质物质的量/mol | 达平衡时体系能量的变化 | ||
| X2 | Y2 | XY3 | ||
| ① | 1 | 3 | 0 | 放热46.3 kJ |
| ② | 0.8 | 2.4 | 0.4 | Q(Q>0) |
下列叙述不正确的是
A.容器①中达到平衡时,Y2的转化率为50%
B.Q="27.78" kJ
C.若容器①体积改为1.0 L.则达平衡时放出的热量大于46.3 kJ
D.容器①、②中反应的平衡常数相等,K=
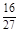
对于化学反应方向的确定,下列说法正确的是( )
| A.在温度、压强一定的条件下,焓因素和熵因素共同决定一个化学反应的方向 |
| B.温度、压强一定时,吸热的熵增反应一定能够自发进行 |
| C.反应焓变是决定反应能否自发进行的唯一因素 |
| D.固体的溶解过程与熵变无关 |
某温度时,在密闭容器中,X、Y、Z三种气体浓度的变化如图Ⅰ所示,若其它条件不变,当温度分别为T1和T2时,Y的体积分数与时间关系如图Ⅱ所示。则下列结论正确的是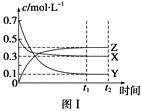
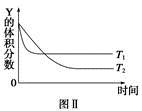
A.该反应的热化学方程式为X(g)+3Y(g)  2Z(g) ΔH>0 2Z(g) ΔH>0 |
| B.若其它条件不变,升高温度,正、逆反应速度均增大,X的转化率减小 |
| C.达到平衡后,若其他条件不变,减小容器体积,平衡向逆反应方向移动 |
| D.达到平衡后,若其他条件不变,通入稀有气体,平衡向正反应方向移动 |
下列关于判断过程的方向的说法正确的是( )
| A.所有自发进行的化学反应都是放热反应 |
| B.高温高压下可以使石墨转化为金刚石的过程是自发过程 |
| C.综合考虑焓变和熵变将更适合于所有的过程 |
| D.同一物质的固、液、气三种状态的熵值相同 |
合成氨反应的正反应是气体体积减小的放热反应。合成氨工业的生产流程如下: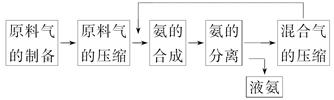
关于合成氨工业的说法中不正确的是( )
| A.混合气进行循环利用遵循绿色化学思想 |
| B.合成氨反应须在低温下进行 |
| C.对原料气进行压缩是为了增大原料气的转化率 |
| D.使用催化剂可以提高反应的速率,但是不能使平衡向正反应方向移动 |
下列各组物质的变化不能用勒夏特列原理解释的是( )
| A.氯水在光照条件下颜色变浅最终变为无色 |
| B.将FeS固体投入到含有Cu2+的废水中以除去Cu2+ |
| C.500 ℃时比室温更利于合成氨 |
| D.乙酸乙酯的合成中用浓硫酸比稀硫酸更有利于乙酸乙酯的生成 |
下列说法可以证明反应N2(g)+3H2(g) 2NH3(g)已达到平衡状态的是( )
2NH3(g)已达到平衡状态的是( )
| A.1个N≡N键断裂的同时,有3个H—H键形成 |
| B.1个N≡N键断裂的同时,有3个H—H键断裂 |
| C.N2、H2、NH3的分子数之比为1∶3∶2 |
| D.1个N≡N键断裂的同时,有6个H—N键形成 |