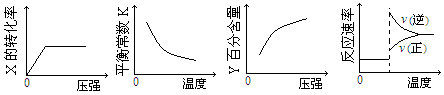
如图为某化学反应的速率与时间的关系示意图。在t1时刻升高温度或增大压强,速率的变化都符合示意图的反应是
A.2SO2(g)+O2(g) 2SO3(g)ΔH<0 2SO3(g)ΔH<0 |
B.4NH3(g)+5O2(g) 4NO(g)+6H2O(g)ΔH<0 4NO(g)+6H2O(g)ΔH<0 |
C.H2(g)+I2(g) 2HI(g)ΔH>0 2HI(g)ΔH>0 |
D.2A(g)+B(s) 2C(g)ΔH>0 2C(g)ΔH>0 |
已知反应2H2(g)+CO(g)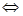 CH3OH(g)的平衡常数如下表。按照相同的物质的量投料,
CH3OH(g)的平衡常数如下表。按照相同的物质的量投料,
测得CO在不同温度下的平衡转化率与压强的关系如下图所示。下列大小比较正确的是
| 平衡常数 | 温度/℃ | ||
| 500 | 700 | 800 | |
| K | 2.50 | 0.34 | 0.15 |
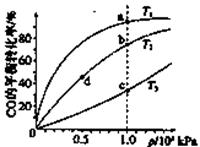
A. 平横常数:K(a)>K(c),K(b)=K(d)
B. 正反应速率:v(a)>v(c),v(b)=v(d)
C. 达到平衡所需时间:t(a)=t(c),t(b)>t(d)
D. 平均相对分子质量:M(a)=M(c),M(b)>M(d)
下列措施对增大反应速率明显有效地是 ( )
| A.Na与水反应时增大水的用量 |
| B.Fe与稀硫酸反应制取氢气时,改用浓硫酸 |
| C.在K2SO4与BaCl2两溶液反应时,增大压强 |
| D.将铝片改为铝粉,做铝与氧气反应的实验 |
在一密闭容器中进行如下反应:2SO2(气)+O2(气) 2SO3(气),已知反应过程中某一时刻SO2、O2、SO3的浓度分别为0.2mol/L、0.1mol/L、0.2mol/L,当反应达平衡时,可能存在的数据是 ( )
2SO3(气),已知反应过程中某一时刻SO2、O2、SO3的浓度分别为0.2mol/L、0.1mol/L、0.2mol/L,当反应达平衡时,可能存在的数据是 ( )
| A.SO2为0.4mol/L、O2为0.2mol/L | B.SO2、SO3均为0.15mol/L |
| C.SO2为0.25mol/L | D.SO3为0.4mol/L |
在密闭容器中进行反应:X(g)+3Y(g)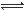 2Z(g),下列说法正确的是 ( )
2Z(g),下列说法正确的是 ( )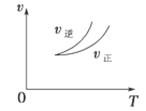
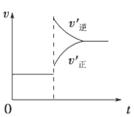
| A.左上图说明正反应为吸热反应 |
| B.反应达平衡后,增大压强气体密度将减小 |
| C.右上图可表示升高温度使平衡向逆反应方向移动 |
| D.右上图虚线可表示使用催化剂后引发的反应速率变化 |
已知N2O4(g)?2NO2(g) △H>0且平衡体系的总质量(m总 )与总物质的量(n总)之比在不同温度下随压强变化曲线如图所示,下列说法正确的是( )
| A.平衡常数K(a)=K(b)<K(c) |
| B.反应速率:va<vb; |
| C.温度:T2>T1 |
D.当 =69g/mol时,若n(NO2):n(N2O4)=2:1, =69g/mol时,若n(NO2):n(N2O4)=2:1, |
-定条件下,在体积为VL的密闭容器中发生如下反应 一段时间后达到化学平衡状态。改变某一条件,下列说法正确的是
一段时间后达到化学平衡状态。改变某一条件,下列说法正确的是
| A.若升高温度,反应混合气体密度不变时即达到新平衡状态 |
| B.若增大B的浓度,△H减小 |
| C.若使用适当催化剂,A的转化率增大 |
| D.若增大压强,平衡向右移动,则m+n>p+q |
用氮化硅陶瓷代替金属制造发动机的耐热部件,能大幅度提高发动机的热效率。工业上用化学气相沉积法制备氮化硅,其反应如下:
3SiCl4 (g) + 2N2 (g) + 6H2 (g)  Si3N4(s) + 12HCl (g) ?H < 0
Si3N4(s) + 12HCl (g) ?H < 0
该反应在恒容的密闭容器中达到平衡后,若仅改变图中横坐标x的值,重新达到平衡后,纵坐标y随x变化趋势合理的是 ( )
| 选项 | x | y |
| A | 温度 | 容器内混合气体的密度 |
| B | N2 的物质的量 | H2的转化率 |
| C | H2的浓度 | 平衡常数K |
| D | 压强 | N2 的转化率 |
 2Z(g);△H<0,达到平衡后,仅改变横坐标条件,下列图像正确的是
2Z(g);△H<0,达到平衡后,仅改变横坐标条件,下列图像正确的是