如图为某化学反应的速率与时间的关系示意图。在t1时刻升高温度或增大压强,速率的变化都符合示意图的反应是: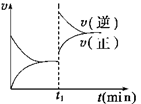
A.2A(g) + B(g) 2C(g) ΔH>0 2C(g) ΔH>0 |
B.2SO2(g)+ O2(g)  2SO3(g)ΔH<0 2SO3(g)ΔH<0 |
C.H2(g) + I2(g)  2HI(g)ΔH>0 2HI(g)ΔH>0 |
D.4NH3(g)+ 5O2(g)  4NO(g) + 6H2O(g)ΔH<0 4NO(g) + 6H2O(g)ΔH<0 |
下列事实不能用勒夏特列原理解释的是
①氯化铁溶液加热蒸干最终得不到氯化铁固体 ②铁在潮湿的空气中容易生锈
③实验室可用排饱和食盐水的方法收集氯气
④常温下,将1 mL pH=3的醋酸加水稀释至100 mL,测得其pH<5
⑤钠与氯化钾共融制备钾:Na(l)+KCl(l)  K(g)+NaCl(l)
K(g)+NaCl(l)
⑥二氧化氮与四氧化二氮的平衡体系,加压后颜色加深
| A.②⑥ | B.①②③ | C.②⑤⑥ | D.①③④⑤ |
工业制硫酸中的一步重要反应是SO2(在400-500 C下的催化氧化:2SO2+O2
C下的催化氧化:2SO2+O2 2SO3,这是一个正反应放热的可逆反应,如果反应在密闭容器中进行,下述有关说法错误的是
2SO3,这是一个正反应放热的可逆反应,如果反应在密闭容器中进行,下述有关说法错误的是
| A.在上述条件下,SO2可能100%的转化为SO3 |
| B.使用催化剂是为了加快反应速率,提高生产效率 |
| C.达到平衡时,SO2与SO3的浓度保持不变 |
| D.为了提高SO2的转化率,可以适当提高O2的浓度 |
用下列方法制取氢气,反应速率最大的是
| A.10℃时,粉末状锌与2 mol·L-1硫酸溶液反应 |
| B.30℃时,粉末状锌与2mol·L-1硫酸溶液反应 |
| C.10℃时,块状锌与2 mol·L-1硫酸溶液反应 |
| D.30℃时,块状锌与2 mol·L-1硫酸溶液反应 |
对于可逆反应2SO2+O2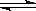 2SO3,在混合气体中充入一定量的18O2,足够长的时间后,18O原子
2SO3,在混合气体中充入一定量的18O2,足够长的时间后,18O原子
| A.只存在于O2中 | B.只存在于O2和SO3中 |
| C.只存在于O2和SO2中 | D.存在于O2、SO2和SO3中 |
用铁片与2mol/L稀硫酸反应制取氢气时,下列措施不能使反应速率加快的是
| A.滴加NaCl溶液 | B.加热 |
| C.换用4mol/L硫酸 | D.换用铁粉 |
 3C(g),在一定条件下,使一定量A和B气体反应,达到平衡状态时,具有的关系是
3C(g),在一定条件下,使一定量A和B气体反应,达到平衡状态时,具有的关系是 降到0.06 mol·L
降到0.06 mol·L 2C(气)达到平衡的标志是
2C(气)达到平衡的标志是 3C+5D反应中,表示该反应速率最快的是
3C+5D反应中,表示该反应速率最快的是