下列有关热化学方程式的叙述,正确的是
| A.1mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热 |
B.由N2O 4(g)  2NO2(g)△H=" -56.9" kJ·mol-1,可知将1mol N2O4(g)置于密闭容器中充分反应后放出热量为56.9kJ 2NO2(g)△H=" -56.9" kJ·mol-1,可知将1mol N2O4(g)置于密闭容器中充分反应后放出热量为56.9kJ |
| C.由:H+(aq)+OH-(aq)=H2O(l)△H=-57.3kJ/mol,可知:含1mol CH3COOH的溶液与含1mol NaOH的溶液混合,放出热量为57.3 kJ |
| D.已知101kPa时,2C(s)+O2(g)===2CO(g) ΔH=-221kJ/mol,则1 mol碳完全燃烧放出的热量大于110.5kJ |
下列图象分别表示有关反应的反应过程与能量变化的关系: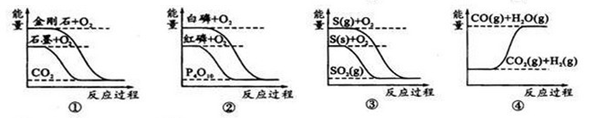
据此判断下列说法正确的是
| A.石墨转变为金刚石是吸热反应 |
| B.白磷比红磷稳定 |
| C.CO(g)+H2O(g)=CO2(g)+H2(g)ΔH>0 |
| D.S(g)+O2(g)=SO2(g) ΔH1; S(s)+O2(g)=SO2(g) ΔH2,则ΔH1>ΔH2 |
下列关于热化学反应的描述中正确的是
| A.HCl和NaOH反应的中加热△H ="-57.3" kJ/mol,则H2SO4和Ca(OH) 2反应的 中和热△H =2×(-57.3)kJ/mol |
B.CO(g)的燃烧热是283.0 kJ/mol,则2CO2(g) 2CO(g)+O2(g)反应 2CO(g)+O2(g)反应的△H =" +2×283.0" kJ/mol |
| C.需要加热才能发生的反应一定是吸热反应 |
| D.1 mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热 |
将1000 mL 0.1 mol·L-1 BaCl2溶液与足量稀硫酸充分反应放出a kJ热量;将1000 mL 0.5 mol·L-1 HCl溶液与足量CH3COONa溶液充分反应放出b kJ热量(不考虑醋酸钠水解);将500 mL 1 mol·L-1 H2SO4溶液与足量(CH3COO)2Ba(可溶性强电解质)溶液反应放出的热量为
| A.(5a-2b) kJ | B.(2b-5a) kJ |
| C.(5a+2b) kJ | D.(10a+4b) kJ |
“天宫一号”目标飞行器与“神舟九号”载人飞船的交会对接,标志着我国具备了建设空间站的基本能力。下列有关说法正确的是
| A.火箭升空的动力主要来源于化学能 |
| B.“神舟九号”飞船的太阳能帆板将太阳能直接转换为动能 |
| C.“天宫一号”中的氢氧燃料电池将电能转换为化学能 |
| D.“天宫一号”利用太阳能将水加热分解为氢气和氧气 |
25℃、101kPa下,2g氢气燃烧生成液态水,放出285.8 kJ热量,表示该反应的热化学方程式正确的是
| A.2H2(g)+O2(g)=2H2O(l)△H=-285.8 kJ/mol |
| B.2H2(g)+O2(g)=2H2O(l)△H=+571.6 kJ/mol |
| C.2H2(g)+O2(g)=2H2O(g)△H=-571.6kJ/mol |
D.H2(g)+ O2(g)=H2O(l)△H=-285.8 kJ/mol O2(g)=H2O(l)△H=-285.8 kJ/mol |
H2和I2在一定条件下能发生反应:H2(g) +I2(g) 2HI(g) △H=—a kJ·mol-1
2HI(g) △H=—a kJ·mol-1
已知: (a、b、c均大于零)
(a、b、c均大于零)
下列说法不正确的是
| A.反应物的总能量高于生成物的总能量 |
| B.断开1 mol H-H键和1 mol I-I键所需能量大于断开2 mol H-I键所需能量 |
| C.断开2 mol H-I键所需能量约为(c+b+a) kJ |
| D.向密闭容器中加入2 mol H2和2 mol I2,充分反应后放出的热量小于2a kJ |
指常温下,1 mol化学键分解成气态原子所需要的能量用E表示。结合表中信息判断下列说法不正确的是
| 共价键 | H-H | F-F | H-F | H-Cl | H-I |
| E(kJ·mol-1) | 436 | 157 | 568 | 432 | 298 |
A.432 kJ·mol-1>E(H-Br)>298 kJ·mol-1
B.表中最稳定的共价键是H—F键
C.H2(g)→2H (g) ?H=+436 kJ·mol-1
D.H2(g)+F2(g)=2HF(g) ?H=—25 kJ·mol-1
生物质(通过光合作用产生的有机体)是一种可再生能源,能发生如下图转化。下列说法不正确的是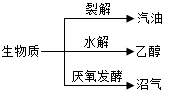
| A.汽油属于纯净物 |
| B.乙醇属于可再生能源 |
| C.沼气的主要成分是甲烷 |
| D.生物质能来源于太阳能 |