题目内容
指常温下,1 mol化学键分解成气态原子所需要的能量用E表示。结合表中信息判断下列说法不正确的是
| 共价键 | H-H | F-F | H-F | H-Cl | H-I |
| E(kJ·mol-1) | 436 | 157 | 568 | 432 | 298 |
A.432 kJ·mol-1>E(H-Br)>298 kJ·mol-1
B.表中最稳定的共价键是H—F键
C.H2(g)→2H (g) ?H=+436 kJ·mol-1
D.H2(g)+F2(g)=2HF(g) ?H=—25 kJ·mol-1
D
解析试题分析:A、Br的非金属性介于Cl、I之间,所以E(H-Br)介于E(H-Cl)、E(H-I)之间,即432 kJ·mol-1>E(H-Br)>298 kJ·mol-1,正确;B、根据表中的数据,H—F键的键能最大,所以表中最稳定的共价键是H—F键,正确;C、破坏化学键需要吸收能量,所以H2(g)→2H (g) ?H=+436 kJ·mol-1,正确;D、H2(g)+F2(g)=2HF(g) ?H=436kJ?mol?1+157kJ?mol?1-2×568kJ?mol?1= -543kJ?mol?1,错误。
考点:本题考查化学反应的热效应。

练习册系列答案
 出彩同步大试卷系列答案
出彩同步大试卷系列答案
相关题目
下列有关化学反应与能量的说法正确的是
| A.酸碱中和是放热反应 |
| B.炭在二氧化碳气体中灼烧发生的反应属于放热反应 |
| C.原子间形成化学键时需吸收能量 |
| D.化学反应过程中,化学能一定全部转化成热能 |
某反应的反应过程中能量变化如右图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能)。对该反应的有关叙述正确的是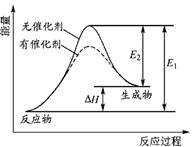
| A.该反应的正反应为吸热反应 |
| B.催化剂能改变反应的焓变 |
| C.催化剂不能降低反应的活化能 |
| D.逆反应的活化能大于正反应的活化能 |
已知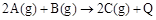 。下列说法或表达正确的是
。下列说法或表达正确的是
| A.使用催化剂可改变该反应的反应热 |
B.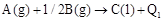 ; ;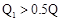 |
C.A和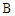 混合气体的稳定性比C气体强 混合气体的稳定性比C气体强 |
| D.该条件下,2LC气体分解成2LA气体与1LB气体吸收的热量为Q |
在压强为2.20×104 kPa、温度达到374℃时,水成为“超临界状态”,此时水可将CO2等含碳化合物转化为有机物,这就是“水热反应”,生物质在地下高温高压条件下通过水热反应可生成石油、煤等矿物能源。下列说法不正确的是( )
| A.二氧化碳与超临界水作用生成汽油的反应,属于放热反应 |
| B.“水热反应”是一种复杂的物理化学变化 |
| C.火力发电厂可望利用废热,将二氧化碳转变为能源物质 |
| D.随着科技的进步,“水热反应”制取能源有望实现地球上碳资源的和谐循环 |
下列关于热化学反应的描述中正确的是
| A.HCl和NaOH反应的中加热△H ="-57.3" kJ/mol,则H2SO4和Ca(OH) 2反应的 中和热△H =2×(-57.3)kJ/mol |
B.CO(g)的燃烧热是283.0 kJ/mol,则2CO2(g) 2CO(g)+O2(g)反应 2CO(g)+O2(g)反应的△H =" +2×283.0" kJ/mol |
| C.需要加热才能发生的反应一定是吸热反应 |
| D.1 mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热 |
已知1g氢气完全燃烧生成水蒸气时放出热量121kJ,且氧气中1molO=O键完全断裂时吸收热量496 kJ,水蒸气1molH-O键形成时放出热量463 kJ,则氢气中1molH-H键断裂时吸收热量为
| A.920 kJ | B.557 kJ | C.436 kJ | D.188 kJ |
信息、材料、能源被称为新科技革命的“三大支柱”。下列观点或做法错误的是
| A.在即将到来的新能源时代,核能、太阳能、氢能将成为主要能源 |
| B.加大煤炭的开采速度,增加煤炭燃料的供应量,以缓解石油危机 |
| C.光缆在信息产业中有广泛应用,制造光缆的主要材料是二氧化硅 |
| D.高温结构陶瓷氮化硅(Si3N4)具有较高的硬度和耐磨性,可用于制造汽车发动机 |
