题目内容
H2和I2在一定条件下能发生反应:H2(g) +I2(g) 2HI(g) △H=—a kJ·mol-1
2HI(g) △H=—a kJ·mol-1
已知: (a、b、c均大于零)
(a、b、c均大于零)
下列说法不正确的是
| A.反应物的总能量高于生成物的总能量 |
| B.断开1 mol H-H键和1 mol I-I键所需能量大于断开2 mol H-I键所需能量 |
| C.断开2 mol H-I键所需能量约为(c+b+a) kJ |
| D.向密闭容器中加入2 mol H2和2 mol I2,充分反应后放出的热量小于2a kJ |
B
解析试题分析:A、△H<0,该反应为放热反应,所以反应物的总能量高于生成物的总能量,正确;B、因为该反应为放热反应,所以断开1 mol H-H键和1 mol I-I键所需能量小于断开2 mol H-I键所需能量,错误;C、设断开2 mol H-I键所需能量为x,则b+c-x=-a,所以x=a+b+c,正确;D、因为该反应为可逆反应,所以向密闭容器中加入2 mol H2和2 mol I2,充分反应后放出的热量小于2a kJ,正确。
考点:本题考查化学反应的热效应。

 中考利剑中考试卷汇编系列答案
中考利剑中考试卷汇编系列答案 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案将盛有NH4HCO3粉末的小烧杯放入盛有少量醋酸的大烧杯中。然后向小烧杯中加入盐酸,反应剧烈,醋酸逐渐凝固。由此可见
| A.复分解反应都是吸热反应 |
| B.NH4HCO3和盐酸的反应是吸热反应 |
| C.反应物的总能量高于生成物的总能量 |
| D.反应的热化学方程式为:NH4HCO3+HCl=NH4Cl+CO2↑+H2O△H>0 |
下列说法正确的是
| A.氢气是一种高效而没有污染的一级能源 |
| B.太阳能、氢能、风能、海洋能、地热能和生物质能等都是新能源 |
| C.CaCO3(s)=CaO(s)+CO2(g)室温下不能自发进行,说明该反应的ΔH<0 |
| D.水的离子积常数Kw随着温度的升高而增大,说明水的电离是放热反应 |
强酸与强碱的稀溶液发生中和反应的热效应:
H+(aq)+ OH-(aq) → H2O (l) +57.3kJ
向1L0.5mol/L的NaOH溶液中加入稀醋酸、浓硫酸、稀硝酸,则恰好完全反应时的热效应Q1、Q2、Q3的关系正确的是
| A.Q1 < Q2 < Q3 | B.Q1 > Q3 > Q2 | C.Q2 > Q1 > Q3 | D.Q1 < Q3 < Q2 |
在同温同压下,下列各组热化学方程式中,△H2>△H1的是
| A.S(g)+O2(g)=SO2(g),△H1; S(s)+O2(g)=SO2(g),△H2 |
| B.2H2(g)+O2(g)=2H2O(g),△H1; 2H2(g)+O2(g)=2H2O(l),△H2 |
C.C(s)+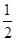 O2(g)=CO(g)△H1;C(s)+O2(g)=CO2(g) △H2 O2(g)=CO(g)△H1;C(s)+O2(g)=CO2(g) △H2 |
| D.H2(g)+Cl2(g)=2HCl(g),△H1; 2H2(g)+2Cl2(g)=4HCl(g),△H2 |
在298 K、100 kPa时,已知:
① 2H2O(g)=O2(g)+2H2(g) ΔH1 ② Cl2(g)+H2(g)=2HCl(g) ΔH2
③ 2Cl2(g)+2H2O(g)=4HCl(g)+O2(g) ΔH3
则ΔH3与ΔH1和ΔH2间的关系正确的是( )
| A.ΔH3=ΔH1+2ΔH2 | B.ΔH3=ΔH1+ΔH2 | C.ΔH3=ΔH1-2ΔH2 | D.ΔH3=ΔH1-ΔH2 |
已知:P4(g)+6Cl2(g)=4PCl3(g) △H=a kJ?mol—1、P4(g)+10Cl2(g)=4PCl5(g) △H=b kJ?mol—1
P4具有正四面体结构,PCl5中P-Cl键的键能为c kJ?mol—1,PCl3中P-Cl键的键能为1.2c kJ?mol—1。下列叙述正确的是
| A.P-P键的键能大于P-Cl键的键能 |
| B.可求Cl2(g)+ PCl3(g)=4PCl5(s)的反应热△H |
| C.Cl-Cl键的键能为(b-a+5.6c)/4 kJ?mol—1 |
| D.P-P键的键能为(5a-3b+12c)/8 kJ?mol—1 |
心脏起搏器电源—锂碘电池的电池反应为:2 Li(s) + I2 (s) =" 2" LiI(s) ΔH
已知:4 Li(s) + O2 (g) =" 2" Li2O(s) ΔH1
4 LiI(s) + O2 (g) =" 2" I2 (s) + 2 Li2O(s) ΔH2 则下列说法正确的是( )
| A.ΔH=1/2ΔH1 -ΔH2 | B.ΔH=1/2ΔH1 +ΔH2 |
| C.ΔH=1/2ΔH1 -1/2ΔH2 | D.ΔH=1/2ΔH1 +1/2ΔH2 |