题目内容
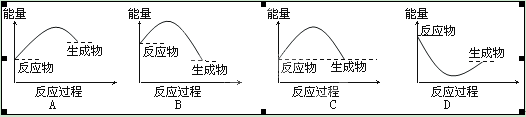
下列关于热化学反应的描述中正确的是
| A.HCl和NaOH反应的中加热△H ="-57.3" kJ/mol,则H2SO4和Ca(OH) 2反应的 中和热△H =2×(-57.3)kJ/mol |
B.CO(g)的燃烧热是283.0 kJ/mol,则2CO2(g) 2CO(g)+O2(g)反应 2CO(g)+O2(g)反应的△H =" +2×283.0" kJ/mol |
| C.需要加热才能发生的反应一定是吸热反应 |
| D.1 mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热 |
B
解析试题分析:A 中加热表示酸碱发生中和反应产生1mol的水时放出的热量。所以无论具体的反应是产生1moL的水还是2mol的水,反应的中和热都是一样的。错误。B CO(g)的燃烧热是283.0 kJ/mol表示的是1mol的CO完全燃烧产生CO2气体的时候所放出的热量。则2mol的CO完全燃烧产生CO2气体放出热量为2×283.0 kJ/mol[。。2CO2(g)分解产生2CO(g)和O2(g)时的吸收的热量与2mol的CO完全燃烧产生CO2气体放出热量数值相等。故2CO2(g)=2CO(g)+O2(g)△H =" +2×283.0" kJ/mol[。。正确。来C.无论是放热反应还是吸热反应都有个断裂旧的化学键,形成新的化学键的过程。因此都有加热补充能量的共存。错误。D.1 mol甲烷燃烧生成液态水和二氧化碳气体时所放出的热量是甲烷的燃烧热。错误。源:Zxxk.Com]
考点:考查反应需要的条件及反应热、中和热、燃烧热等概念机应用的知识。

 名题金卷系列答案
名题金卷系列答案 优加精卷系列答案
优加精卷系列答案已知:H2(g)+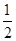 O2(g)=H2O(l) ΔH1=-285.8 kJ·mol-1 ①
O2(g)=H2O(l) ΔH1=-285.8 kJ·mol-1 ①
H2(g)=H2(l) ΔH2=-0.92 kJ·mol-1 ② O2(g)=O2(l) ΔH3=-6.84 kJ·mol-1 ③
H2O(g)=H2O(l) ΔH4=-44 kJ·mol-1 ④
下列说法正确的是
| A.上述四个反应都是吸热反应 |
| B.1 mol液态H2的能量大于1 mol气态H2的能量 |
| C.H2的燃烧热(ΔH)为-285.8 kJ·mol-1 |
D.火箭中液氢燃烧的热化学方程式为H2(l)+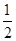 O2(l)=H2O(g) ΔH=-285.8 kJ·mol-1 O2(l)=H2O(g) ΔH=-285.8 kJ·mol-1 |
在一定条件下,CO和CH4燃烧的热化学方程式分别为:2CO(g)+O2(g) =2CO2(g) H=" -566" kJ/mol,CH4(== CO2(g) + 2H2O(l)
H=" -566" kJ/mol,CH4(== CO2(g) + 2H2O(l)  H=" -890" kJ/mol, 由1molCO和3molCH4组成的混合气体在上述条件下完全燃烧时,释放的热量为
H=" -890" kJ/mol, 由1molCO和3molCH4组成的混合气体在上述条件下完全燃烧时,释放的热量为
| A.2912 kJ | B.2953 kJ | C.3236 kJ | D.3867 kJ |
指常温下,1 mol化学键分解成气态原子所需要的能量用E表示。结合表中信息判断下列说法不正确的是
| 共价键 | H-H | F-F | H-F | H-Cl | H-I |
| E(kJ·mol-1) | 436 | 157 | 568 | 432 | 298 |
A.432 kJ·mol-1>E(H-Br)>298 kJ·mol-1
B.表中最稳定的共价键是H—F键
C.H2(g)→2H (g) ?H=+436 kJ·mol-1
D.H2(g)+F2(g)=2HF(g) ?H=—25 kJ·mol-1
知:① 2C(已s)+O2(g) =2CO(g)  H= -221.0kJ/mmol
H= -221.0kJ/mmol
②2H2(g) + O2(g) =2H2O(g)  H= -483.6kJ/ol。
H= -483.6kJ/ol。
则制备水煤气的反应 C(s) +H2O(g) = CO(g) + H2(g)的 H为
H为
| A.+262.6kJ/mol | B.-131.3kJ/mol | C.-352.3kJ/mol | D.+131.3kJ/mol |
在压强为2.20×104 kPa、温度达到374℃时,水成为“超临界状态”,此时水可将CO2等含碳化合物转化为有机物,这就是“水热反应”,生物质在地下高温高压条件下通过水热反应可生成石油、煤等矿物能源。下列说法不正确的是( )
| A.二氧化碳与超临界水作用生成汽油的反应,属于放热反应 |
| B.“水热反应”是一种复杂的物理化学变化 |
| C.火力发电厂可望利用废热,将二氧化碳转变为能源物质 |
| D.随着科技的进步,“水热反应”制取能源有望实现地球上碳资源的和谐循环 |
已知:H+(aq)+OH-(aq) =H2O(l); △H=-57.3 kJ·mol-1。现将一定量的稀盐酸、浓硫酸、稀醋酸分别和1L 1mol·L-1的NaOH溶液恰好完全反应,其反应热分别为△H1、△H2、△H3,,则△H1、△H2和△H3的大小关系为
| A.△H1=△H2 | B.△H2>△H1 |
| C.△H3>△H2 | D.△H1>△H3 |
下列有关热化学方程式的叙述中,正确的是 ( )
| A.含20.0g NaOH的稀溶液与足量的稀硫酸完全中和,放出28.7kJ的热量,则表示中[和热的热化学方程式为2NaOH(aq)+H2SO4(aq)=Na2SO4(aq)+2H2O(l)△H=-114.8kJ/mol |
B.已知热化学方程式:SO2(g)+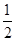 O2(g) O2(g) SO3(g) △H=-98.32kJ/mol,在容器中充入2molSO2和1molO2充分反应,最终放出的热量为196.64kJ SO3(g) △H=-98.32kJ/mol,在容器中充入2molSO2和1molO2充分反应,最终放出的热量为196.64kJ |
| C.已知2H2(g)+O2(g)=2H2O(g); △H=-483.6kJ/mol,则H2的燃烧热为241.8kJ/mol |
| D.已知①S(s)+O2(g)=SO2(g); △H1②S(g)十O2(g)=SO2(g);△H2 则△H1>△H2 |