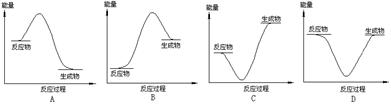
已知25℃、101kPa条件下:
4Al (s) + 3O2 (g)=2Al2O3 (s) △H=-2834.9 kJ/mol
4Al (s) + 2O3 (g) = 2Al2O3 (s) △H= -3119.91kJ/mol
由此得出的结论正确的是
| A.等质量的O2比O3能量低,由O2变O3为放热反应 |
| B.等质量的O2比O3能量低,由O2变O3 为吸热反应 |
| C.3O2(g)=2O3 (g)△H=285.0 kJ/mol |
| D.O3比O2稳定,由O2变O3 为吸热反应 |
某反应过程中能量变化如下图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能)。下列有关叙述正确的是
| A.催化剂能降低反应的活化能 |
| B.催化剂能改变反应的焓变(△H) |
| C.该反应为放热反应 |
| D.正反应的活化能小于逆反应的活化能 |
根据下图,下列判断中正确的是
| A.烧杯a中的溶液pH不变 |
| B.烧杯a中发生氧化反应 |
| C.烧杯a中发生的反应为2H2O+2e-=H2↑+2OH- |
| D.烧杯b中发生的反应为Zn-2e-=Zn2+ |
下列反应过程中的能量变化与下图一致的是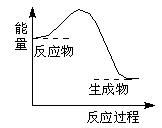
A.2Al+Fe2O3 2Fe+Al2O3 2Fe+Al2O3 |
B.C+CO2 2CO 2CO |
C.CaCO3 CaO+CO2↑ CaO+CO2↑ |
D.C+H2O CO+H2 CO+H2 |
对于化学反应中的能量变化,表述准确的是
| A.形成新化学键的过程会放出能量 | B.中和反应是吸热反应 |
| C.加热才能发生的反应是吸热反应 | D.生成CO2的反应是放热反应 |
关于吸热反应的说法,正确的是
| A.凡需加热的反应一定是吸热反应 |
| B.只有分解反应才是吸热反应 |
| C.使用催化剂的反应是吸热反应 |
| D.酸碱中和反应的逆反应是吸热反应 |
根据热化学方程式:S(g)+O2(g) SO2(g) △H=-QkJ·mol-1(Q>0),下列分析正确的是( )
SO2(g) △H=-QkJ·mol-1(Q>0),下列分析正确的是( )
| A.1 mol S(g)与1 mol O2(g)反应生成1 mol SO2(g)放出QkJ的热量 |
| B.1个S(g)与1个O2(g)完全反应要放出Q kJ的热量 |
C.S(s)+O2(g) SO2(g) △H<-Q kJ·mol-1 SO2(g) △H<-Q kJ·mol-1 |
| D.1 mol S(g)与1 mol O2(g)的总能量比1 mol SO2(g)的总能量低QkJ |
下列反应前后物质的总能量变化可用如图表示的是( )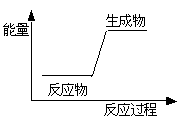
| A.生石灰加水生成熟石灰 |
| B.C+H2O=CO+H2 |
| C.金属钠与水反应 |
| D.HNO3+NaOH=NaNO3+H2O |
对于反应中的能量变化,表述正确的是
| A.断开化学键的过程会放出能量 |
| B.放热反应中,反应物的总能量大于生成物的总能量 |
| C.加热才能发生的反应一定是吸热反应 |
| D.氧化反应均为吸热反应 |