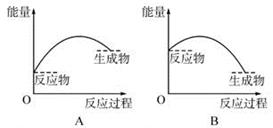
CO(g)+H2O(g)  H2(g)+CO2(g) △H<0,在其他条件不变的情况下,下列说明正确的是
H2(g)+CO2(g) △H<0,在其他条件不变的情况下,下列说明正确的是
| A.加入催化剂,改变了反应的途径,反应放出的热量也随之改变 |
| B.改变压强,平衡不发生移动,反应放出的热量不变 |
| C.升高温度,反应速率加快,反应放出的热量不变 |
| D.若在原电池中进行,反应放出的热量不变 |
某实验小组学生用50mL0.50mol/L的盐酸与50mL0.55mol/L的NaOH溶液在如图所示的装置中进行中和反应、通过测定反应过程中所放出的热量计算反应热.下列说法正确的是
| A.如图条件下实验过程中没有热量损失 |
| B.若改用60ml0.50mol/L盐酸跟50ml0.55mol/L的NaOH溶液进行反应,通过测定反应过程中所放出的热量相等 |
| C.图中实验装置缺少环形玻璃搅拌棒 |
| D.烧杯间填满碎纸条的作用是固定小烧杯。 |
下列关于化学反应与能量的说法正确的是
| A.中和反应是吸热反应 |
| B.燃烧是放热反应 |
| C.化学键断裂放出能量 |
| D.反应物总能量与生成物总能量一定相等 |
下列反应既属于氧化还原反应,又是吸热反应的是
| A.铝与稀盐酸的反应 |
| B.灼热的木炭与CO2反应 |
| C.甲烷在氧气中的燃烧反应 |
| D.Ba(OH)2·8H2O晶体与NH4Cl晶体的反应 |
在101kPa 25℃时,1.0g乙烷气体完全燃烧生成液态水时放出热量52.0kJ,则乙烷燃烧的热化学方程式为
A.C2H6(g) + 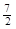 O2(g)=2CO2(g) +3H2O(l)△H =-1560kJ·mol-1 O2(g)=2CO2(g) +3H2O(l)△H =-1560kJ·mol-1 |
| B.2C2H6(g) + 7O2(g)=4CO2(g) +6H2O(g)△H =-1560kJ·mol-1 |
| C.2C2H6(g) + 7O2(g)=4CO2(g) +6H2O(l)△H =+3120 kJ·mol-1 |
D.C2H6(g) +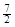 O2(g)=2CO2(g) +3H2O(l)△H =-52.0kJ·mol-1 O2(g)=2CO2(g) +3H2O(l)△H =-52.0kJ·mol-1 |
反应A(g)+2B(g)===C(g)的反应过程中能量变化如下图所示。下列相关说法正确的是
| A.该反应是吸热反应 |
| B.催化剂改变了该反应的焓变 |
| C.曲线b表示使用催化剂后的能量变化 |
| D.该反应的焓变ΔH= -510 kJ·mol-1 |
下列属于吸热反应的是
| A.CaO + H2O = Ca(OH)2 | B.C + H2O CO + H2 CO + H2 |
| C.NaOH + HCl =" NaCl" + H2O | D.2Mg + CO2 2MgO + C 2MgO + C |
对于放热反应H2 + Cl2  2HCl,下列说法正确的是
2HCl,下列说法正确的是
| A.该反应涉及到了离子键和共价键的断裂与形成 |
| B.反应物所具有的总能量高于产物所具有的总能量 |
| C.断开1 mol H—H键和1 mol Cl—Cl键,所吸收的总能量,小于形成1 mol H—Cl键,所放出的能量 |
| D.该反应中,化学能只转变为热能 |
已知298 K时,合成氨反应N2(g)+3H2(g)  2NH3(g) ΔH=-92.0 kJ·mol-1,将此温度下的1 mol N2和3 mol H2放在一密闭容器中,在催化剂存在时进行反应。测得反应放出的热量为(假定测量过程中没有能量损失) ( )
2NH3(g) ΔH=-92.0 kJ·mol-1,将此温度下的1 mol N2和3 mol H2放在一密闭容器中,在催化剂存在时进行反应。测得反应放出的热量为(假定测量过程中没有能量损失) ( )
| A.一定小于92.0 kJ | B.一定大于92.0 kJ |
| C.一定等于92.0 kJ | D.无法确定 |