下图是短周期元素原子半径与最外层电子数的关系图,其中乙单质是半导体,下列说法正确的是( )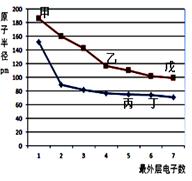
| A.丙的氢化物与丙的最高价氧化物的水化物能发生化合反应 |
| B.气态氢化物的稳定性:丙>丁>戊 |
| C.甲的离子半径比丁的简单离子半径小 |
| D.乙与丁形成的化合物含共价键,同时是两性氧化物 |
1~18号元素的离子aW3+、bX+、cY2-、dZ-都具有相同的电子层结构,下列关系正确的是
| A.质子数b>c | B.离子的还原性Y2-< Z- |
| C.原子半径X<W | D.氢化物的稳定性H2Y>HZ |
X是第三周期非金属元素,该原子如果要达到8电子稳定结构,需要的电子数小于其次外层和最内层的电子数之差,且等于最内层电子数的整数倍。下列说法正确的是
| A.X最高价氧化物对应的水化物不一定是强酸 |
| B.X元素的氢化物化学式一定为H2X |
| C.X的单质—定是良好的半导体材料 |
| D.X元素的氧化物—定能与烧碱反应 |
X、Y、Z、W为四种短周期主族元素,它们在周期表中的相对位置如下图所示。Z元素原子核外K层与M层电子数相等。下列说法中正确的
| | | X | Y |
| Z | W | | |
A.Y元素最高价氧化物对应的水化物化学式为H3YO4
B.原子半径由小到大的顺序为:X<Z<Y<W
C.与同浓度的盐酸反应,Z比W更剧烈
D.X的氧化物不能与Z单质反应
同周期的X、Y、Z三种元素,常温下它们的气态氢化物的化学式为H2X、YH3、ZH4,下列说法正确的是( )
| A.气态氢化物的稳定性按X、Y、Z的顺序递减 |
| B.三种元素的含氧酸酸性:H4ZO4 > H3YO4> H2XO4 |
| C.元素的最高正价按X、Y、Z的顺序递减 |
| D.元素原子的半径按X、Y、Z的顺序递减 |
下列叙述中,不能肯定金属A 比金属 B的活泼性强的是( )
| A.A能与热水反应产生H2,B 必须与水蒸气反应才产生H2 |
| B.A和B都是元素周期表的主族金属元素,A在 B的左下方 |
| C.1mol A能从酸中置换出1.5molH2,1mol B能从酸中置换出1molH2 |
| D.A和B都是元素周期表的主族金属元素,B的最高价氧化物的水化物不溶于水且具有两性,能被A的最高价氧化物的水化物溶解 |
现代医学证明,硒是人体中14种必需的营养元素之一,缺硒与贫血、冠心病、不孕症、癌症等疾病直接相关。因此,硒被誉为“生命的奇效元素”。已知硒元素与氧元素同主族,则下列关于硒的叙述中不正确的是( )
| A.H2Se比H2O稳定 |
| B.最高价氧化物的水化物化学式为H2SeO4 |
| C.它有两种氧化物SeO2和SeO3 |
| D.其单质常温下呈固态 |
aXn-和 bYm+为两种主族元素的离子,它们的核外电子排布相同,下列判断中正确的是( )
| A.原子序数:X>Y | B.a -n = b+m |
| C.离子半径:Xn-> Ym+ | D.原子半径:X>Y |