题目内容
同周期的X、Y、Z三种元素,常温下它们的气态氢化物的化学式为H2X、YH3、ZH4,下列说法正确的是( )
| A.气态氢化物的稳定性按X、Y、Z的顺序递减 |
| B.三种元素的含氧酸酸性:H4ZO4 > H3YO4> H2XO4 |
| C.元素的最高正价按X、Y、Z的顺序递减 |
| D.元素原子的半径按X、Y、Z的顺序递减 |
AC
解析试题分析:气态氢化物中氢元素显+1价,则X、Y、Z的最低负价分别为—2、—3、—4,由于最低负价=主族序数—8(除氢外),则X、Y、Z分别位于同周期的第VIA、VA、IVA族,非金属性:X>Y>Z,则气态氢化物的稳定性:H2X>YH3>ZH4,故A正确;非金属行越强,最高价氧化物对应水化物酸性越强,则酸性:H4ZO4 < H3YO4< H2XO4,故B错;X、Y、Z的最低负价分别为—2、—3、—4,由于主族元素的最高正价=最低负价+8(除氢外),则X、Y、Z的最高正价分别为+6、+5、+4,故C正确;X、Y、Z的原子序数逐渐减小,同周期主族元素的原子序数越大,其原子半径越小,则X、Y、Z的原子半径逐渐增大,故D错。
考点:考查元素在周期表中位置与元素及其化合物性质的推断,涉及同周期非金属气态氢化物的化学式、主族非金属元素的最低负价、主族序数、原子序数、最高正价、非金属性强弱、气态氢化物稳定性强弱、最高价氧化物对应水化物酸性强弱、原子半径大小比较等。

 一卷搞定系列答案
一卷搞定系列答案 名校作业本系列答案
名校作业本系列答案 轻巧夺冠周测月考直通名校系列答案
轻巧夺冠周测月考直通名校系列答案氧元素是地壳中含量最多的元素。下列说法正确的是
| A.16O2与18O3互为同位素 |
| B.氧元素与其它短周期非金属元素形成的氧化物均属于酸性氧化物 |
| C.O2变成O3以及16O变成18O的变化均属于化学变化 |
| D.氧与钠形成的稳定化合物中,阴、阳离子个数比均为1∶2 |
下图是部分短周期主族元素原子半径与原子序数的关系图。则下列说法正确的是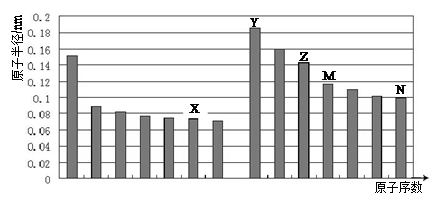
| A.Z、N两种元素的离子半径相比,前者较大 |
| B.X、N两种元素的气态氢化物的稳定性相比,前者较弱 |
| C.由X与M两种元素组成的化合物不能与任何酸反应,但能与强碱反应 |
| D.Z的氧化物能分别溶解于Y的氢氧化物和N的氢化物的水溶液 |
短周期元素Q、R、T、W在元素周期表中的位置如右图所示,其中T所处的周期序数与主族序数相等,下列推断正确的是
| | Q | R | |
| T | | | W |
A.T的氧化物是光导纤维的主要成分
B.W的氢化物的化学式为HCl
C.R的最高正价氧化物的水化物是弱电解质
D.Q与氢形成的化合物均含极性共价键
下图是部分短周期元素原子(用字母表示)最外层电子数与原子序数的关系图。下列说法正确的是
| A.X和R在同一周期 |
| B.原子半径:W>R>X |
| C.气态氢化物的稳定性:Y>X |
| D.X、Z形成的化合物中可能含有共价键 |
X、Y、Z是原子序数依次递增的短周期元素,3种元素的原子核外电子数之和与Ca2+的核外电子数相等,X、Z分别得到一个电子后均形成稀有气体原子的稳定电子层结构。下列说法正确的是
| A.原子半径:Z>Y>X |
| B.Z与X形成化合物的沸点高于Z的同族元素与X形成化合物的沸点 |
| C.Na2Y2与水发生氧化还原反应时,Na2Y2只作氧化剂 |
| D.CaX2、CaY2和CaZ2等3种化合物中,阳离子与阴离子个数比均为1︰2 |
16O中的16表示的含义是( )
| A.氧元素的相对原子质量 |
| B.氧元素的一种同位素的近似相对原子质量 |
| C.氧元素的近似相对原子质量 |
| D.氧元素的一种同位素的质量数 |