X、Y、Z、W是原子序数依次增大的短周期主族元素,X与Z同主族,X原子的最外层电子数是其最内层电子数的2倍,Y原子的最外层电子数比W原子的少2个。下列叙述一定正确的是
| A.X、Y的单质均可以导电 |
| B.原子半径:Z>W |
| C.X、Z的氧化物均为酸性氧化物 |
| D.Y、W的最高价氧化物的水化物均易溶于水 |
短周期元素X、Y、Z、W、Q在周期表中的位置如图所示。下列说法不正确的是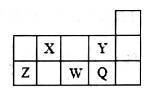
| A.元素的非金属性Y>Q,但其同浓度氢化物水溶液的酸性,HY<HQ |
| B.形成简单离子的半径从小到大的顺序是Y<Q<W |
| C.Z的最高价氧化物可溶于水,也能溶于强碱溶液 |
| D.X的气态氢化物浓溶液可用于检验管道氯气的泄漏 |
元素的原子结构决定其性质和在周期表中的位置,下列说法正确的是
| A.元素周期表中位于金属和非金属分界线附近的元素属于过渡元素 |
B.某微粒的结构示意简图为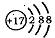 ,则该元素在周期表中位于第三周期、VIA族 ,则该元素在周期表中位于第三周期、VIA族 |
| C.Be(OH)2的碱性比Mg(OH)2的碱性强 |
| D.原子半径:Na>Si>O |
下列说法中,正确的是
| A.H35Cl、H37Cl属于同素异形体 |
| B.16O与18O的中子数不同,核外电子排布却相同 |
| C.稳定性:CH4>SiH4;还原性:HCl>H2S |
| D.K+、Ca2+、Mg2+的离子半径依次增大,还原性依次增强 |
已知几种短周期元素的原子半径、常见的最高价和最低价如下表,下列说法下正确的是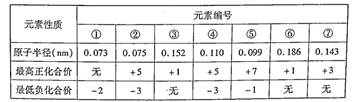
| A.⑦的简单离子不是同周期元素离子半径最小的 |
| B.气态氢化物的稳定性①>② |
| C.②的气态氢化物浓溶液可用于检验氯气管道的泄漏 |
| D.阴离子的还原性④大于⑤,最高价氧化物的水化物的碱性③小于⑥ |
氧元素是地壳中含量最多的元素。下列说法正确的是
| A.16O2与18O3互为同位素 |
| B.氧元素与其它短周期非金属元素形成的氧化物均属于酸性氧化物 |
| C.O2变成O3以及16O变成18O的变化均属于化学变化 |
| D.氧与钠形成的稳定化合物中,阴、阳离子个数比均为1∶2 |
下列说法正确的是
| A.非金属元素组成的化合物中只可能含有共价键 |
| B.ⅦA族元素气态氢化物的热稳定性和还原性从上到下依次减弱 |
| C.第三周期非金属元素最高价含氧酸的酸性从左到右依次增强 |
| D.元素周期表中位于金属和非金属分界线附近的元素属于过渡元素 |
甲、乙、丙、丁为4种短周期元素,在周期表中,甲与乙、丙、丁在周期表中的位置关系如图所示(原子序数:乙>丙)。丁的原子序数与乙、丙原子序数之和相等,4种元素原子的最外层电子数之和为24。下列判断正确的是 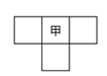
| A.元素甲的简单气态氢化物稳定性比乙的强 |
| B.元素丁在周期表中的位置为第3周期,VIA族 |
| C.元素丙和元素丁的最高价氧化物对应的水化物均为强酸 |
| D.4种元素的简单阴离子半径从大到小顺序为:丁>乙>丙>甲 |
Q、W、X、Y、Z是原子序数依次增大的短周期元素,X的焰色反应呈黄色。Q元素
的原子最外层电子数是其内层电子数的2倍。W、Z最外层电子数相同,Z的核电荷数是W的2倍。元素Y的合金是日常生活中常用的金属材料。下列说法正确的是
| A.原子半径的大小顺序:rX> rY> rW> rQ |
| B.元素Q和Z能形成QZ2型的共价化合物 |
| C.工业上常用电解的方法制备X、Y的单质 |
| D.X、Y的最高价氧化物的水化物之间不能反应 |