几种短周期元素的原子半径及主要化合价如下表:
| 元素代号 | X | Y | Z | M | R |
| 原子半径/nm | 0.186 | 0.102 | 0.075 | 0.074 | 0.143 |
| 主要化合价 | +1 | +6 -2 | +5 -3 | -2 | +3 |
已知X是短周期中最活泼的金属,且与R同周期。下列叙述错误的是( )
A.离子半径大小:Y2- > M2- > R3+
B.Z与M组成的化合物是形成酸雨的原因之一
C.将YM2通入BaCl2溶液中有大量白色沉淀产生
D.X、Y、R的最高价氧化物的水化物两两之间能发生反应
X、Y、Z、R、W是5种短周期元素,原子序数依次增大,它们可组成离子化合物Z2Y和共价化合物RY3、XW4,已知Y、R同主族,Z、R、W同周期。下列说法不正确的是
| A.原子半径:Z>R>W |
| B.X2W6分子中各原子均满足8电子结构 |
| C.气态氢化物的稳定性:HmW>HnR |
| D.Y、Z形成的化合物中只可能存在离子键 |
E、F、G、M是原子序数依次增大的短周期主族元素,E、G在周期表中的相对位置如下表。已知E元素最低负化合价的绝对值与其原子最外层电子数相等,F是地壳中含量最多的金属元素。下列说法错误的是( )
| E | | |
| | | G |
A.E和氢组成的化合物分子中只含有极性共价键
B.工业上用电解熔融的F的氧化物方法来制备F
C.G、M两元素的气态氢化物中,M的气态氢化物更稳定
D.E、F、G、M元素最高价氧化物对应的水化物中酸性最强的是M的最高价含氧酸
已知1~18号元素的离子aW2+、bX+、cY2-、dZ-都具有相同的电子层结构,下列关系正确的是。
| A.离子半径 W2+>X+ | B.离子的还原性Y2->Z- |
| C.氢化物的稳定性 H2Y>HZ | D.原子半径 X < W |
下列具有特殊性能的材料中,由主族元素和副族元素形成的化合物是
| A.半导体材料砷化镓 | B.透明陶瓷材料硒化锌 |
| C.吸氢材料镧镍合金 | D.超导材料K3C60 |
下列各组关系正确的是:
| A.原子半径 N<P<S | B.稳定性 NH3<H2O<HF |
| C.碱性 NaOH>KOH | D.酸性 H3AsO4>H2SeO4>HBrO4 |
Rn+离子有m个电子,它的质量数为A,则原子核内的中子数为 ( )
| A.m +n | B.A-m+n | C.A-m-n | D.A+m-n |
现有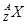 和
和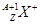 两种粒子,下列叙述正确的是
两种粒子,下列叙述正确的是
| A.质子数相等 |
| B.X元素的质量数为A |
C.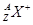 一定具有稀有气体元素原子的核外电子排布 一定具有稀有气体元素原子的核外电子排布 |
| D.它们的化学性质几乎完全相同 |
2013年2月朝鲜进行了第三次核试验,引起国际社会的极大关注。235 92U是一种重要的核燃
料,235 92U和 238 92U的关系是
| A.中子数相同 | B.同种原子 | C.同位素 | D.同种核素 |
短周期主族元素X、Y、Z、W、Q的原子序数依次增大,X的气态氢化物极易溶于Y的氢化物中,常温下,Z的单质能溶于W的最高价氧化物的水化物的稀溶液,却不溶于其浓溶液。下列说法正确的是
| A.元素Y的最高正化合价为+6 |
| B.离子半径的大小顺序为W>Q>Z>X>Y |
| C.氢化物的沸点Y>W |
| D.元素W的最高价氧化物对应水化物的酸性比Q的强 |