题目内容
X、Y、Z、R、W是5种短周期元素,原子序数依次增大,它们可组成离子化合物Z2Y和共价化合物RY3、XW4,已知Y、R同主族,Z、R、W同周期。下列说法不正确的是
| A.原子半径:Z>R>W |
| B.X2W6分子中各原子均满足8电子结构 |
| C.气态氢化物的稳定性:HmW>HnR |
| D.Y、Z形成的化合物中只可能存在离子键 |
D
解析试题分析:X、Y、Z、R、W是5种短周期元素,原子序数依次增大,离子化合物Z2Y中Z的化合价为+1价,Y的化合价为-2价,分别为ⅠA族和ⅥA族元素,已知Y、R同主族,且形成共价化合物RY3,则R为S元素,Y为O元素,Z、R、W同周期,则Z为Na元素;W原子序数比R大,则W是Cl元素,根据XW4可知X为C元素,综上所述X、Y、Z、R、W分别是C、O、Na、S、Cl。 A、根据同周期元素从左到右原子半径逐渐减小,Z、R、W同周期,分别为Na、S、Cl,原子半径逐渐减小,正确; B、X2W6的分子式为C2Cl6,为六氯乙烷,分子中每个C原子形成4个共价键,C原子最外层满足8电子稳定结构,Cl形成1个共价键,最外层电子数也为8,正确;C、根据同周期由左向右气态氢化物的稳定性逐渐增强,则氢化物稳定性HCl>H2S,正确;D、Y、Z可形成的化合物为Na2O和Na2O2,Na2O2中既含离子键又含共价键,错误。
考点:考查元素推断、递变规律和相关物质的结构与性质。

能说明氯的非金属性比溴强的事实是( )
①共用电子对偏移程度:H-Cl > H-Br ②酸性:HClO4 > HBrO4
③热稳定性:HCl > HBr ④酸性:HCl <HBr
| A.①②③ | B.①②④ | C.②③④ | D.②③ |
下列各组给定原子序数的元素,能形成原子数之比为1∶1稳定化合物的是( )
① 1和6 ② 7和8 ③ 8 和 12 ④ 12和17 ⑤ 20和35
| A.①②④ | B.②③⑤ | C.①②③ | D.③④⑤ |
Rn+离子有m个电子,它的质量数为A,则原子核内的中子数为 ( )
| A.m +n | B.A-m+n | C.A-m-n | D.A+m-n |
短周期元素X、Y、Z、W 的原子序数依次增大,且原子最外层电子数之和为13。X 的原子半径比Y 的小,X 与W 同主族,Z 是地壳中含量最高的元素。下列说法正确的是( )
| A.原子半径的大小顺序: r(Y)>r(Z)>r(W) |
| B.元素Z、W 的简单离子的电子层结构不同 |
| C.元素Y 的简单气态氢化物的热稳定性比Z 的强 |
| D.只含X、Y、Z 三种元素的化合物,可能是离子化合物,也可能是共价化合物 |
实际存在的11H、12H、13H 、H+和H2,它们是
| A.氢的五种同位素 | B.氢元素的五种不同微粒 | C.氢的五种核素 | D.五种氢元素 |
由短周期元素组成的甲、乙、丙、丁四种物质分别含有两种以上元素,它们的分子质子总数均与氩原子相同。已知甲是气态氢化物,在水中分步电离出两种阴离子。下列推断合理的是 ( )
| A.某钠盐溶液含甲电离出的阴离子,则该溶液显碱性,只能与酸反应 |
| B.乙与氧气的摩尔质量相同,则乙一定含有极性键和非极性键 |
| C.丙中含有第二周期IV A族的元素,则丙一定是甲烷的同系物 |
| D.丁和甲中各元素质量比相同,则丁中一定含有-1价的元素 |
短周期元素X、Y、Z、W在元素周期表中的相对位置如下图所示。下列说法正确的是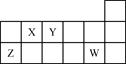
| A.原子半径的大小顺序:rZ>rY>rX |
| B.氢化物的稳定性强弱顺序:XH4>YH3>HW |
| C.Y的氢化物与W的氢化物化合所得产物中只含有共价键 |
| D.X、Y、Z、W四种元素的最高价氧化物对应水化物均能与强碱反应 |