短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中W原子的最外层电子数是最内层电子数的3倍。下列判断正确的是 ( )。
| A.原子半径:r(W)>r(Z)>r(Y)>r(X) |
| B.含Y元素的盐溶液有的显酸性,有的显碱性 |
| C.最简单气态氢化物的热稳定性:Z>W |
| D.X与氢元素组成的化合物XH5与水反应可产生两种气体 |
元素R、X、T、Z、Q在元素周期表中的相对位置如表所示,其中R单质在暗处与H2剧烈化合并发生爆炸,则下列判断正确的是( )。
| A.非金属性:Z<T<X |
| B.R与Q的电子数相差26 |
| C.气态氢化物稳定性:R<T<Q |
| D.最高价氧化物的水化物的酸性:T>Q |
根据不同的研究目的,可以编制成不同的元素周期表。将前18号元素按原子序数递增的顺序排列,可形成如图所示的“蜗牛”元素周期表,图中每个“.”代表一种元素,其中P点代表氢元素(图中的字母不表示元素符号)。下列说法正确的是
| A.Y点元素对应的氢化物比z点元素对应的氢化物更稳定 |
| B.虚线相连的两个点元索处于同一族 |
| C.比Y点原子序数小8的元素,它的最高氧化物对应的水化物是一种弱酸 |
D.K、L、X三种元素的离子半径大小顺序是X3+> >K2- >K2- |
根据下表(部分短周期元素的原子半径及主要化合价)信息,下列叙述正确的是 ( )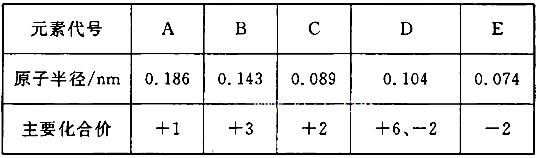
| A.E2-与B3+的核外电子数不可能相等 |
| B.离子半径大小A+<E2- |
| C.最高价氧化物对应水化物的碱性A<C |
| D.氢化物的稳定性H2D>H2E |
某短周期金属元素原子核外最外层电子数是最内层电子数的1.5倍,下列说法正确的是( )
| A.该元素的单质性质活泼,具有较强的还原性,可以用于某些金属冶炼 |
| B.该元素的单质常温下不与浓硫酸反应 |
| C.该元素的单质无需特别保存,因为其性质稳定,不易与空气中的成分反应 |
| D.该元素的最高价氧化物对应的水化物只能与酸反应 |
下列说法中,正确的是 ( )
A.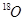 原子核内的中子数为8 原子核内的中子数为8 |
B.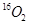 和 和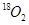 的化学性质几乎相同 的化学性质几乎相同 |
C.H2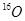 与H2 与H2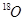 质子数不同 质子数不同 |
| D.H2和D2属于同位素 |
下列说法正确的是
| A.N和As属于第VA族元素,N原子得电子能力比As原子强 |
| B.族序数等于其周期序数的元素一定是金属元素 |
| C.元素周期表中,位于金属和非金属交界线附近的元素属于过渡元素 |
| D.Si、S、Cl的最高价氧化物都能与水反应生成相应的酸,且酸性依次增强 |
X、Y、Z、W均为短周期元素,它们在周期表中的位置如图所示。若Y原子的最外层电子数是内层电子数的3倍,下列说法中正确的是 
| A.原子半径:W>Z>Y>X |
| B.相等物质的量浓度的气态氢化物溶液的pH: X>Z>W |
| C.最高价氧化物对应水化物的酸性:Z>W>X |
| D.四种元素的单质中,Z单质的熔沸点最低 |

