题目内容
X、Y、Z、W均为短周期元素,它们在周期表中的位置如图所示。若Y原子的最外层电子数是内层电子数的3倍,下列说法中正确的是 
| A.原子半径:W>Z>Y>X |
| B.相等物质的量浓度的气态氢化物溶液的pH: X>Z>W |
| C.最高价氧化物对应水化物的酸性:Z>W>X |
| D.四种元素的单质中,Z单质的熔沸点最低 |
B
解析试题分析:X、Y、Z、W均为短周期元素,Y原子的最外层电子数是内层电子数的3倍,则Y原子有2个电子层,所以Y为氧元素,根据X、Y、Z、W在周期表中相对位置可知,X为氮元素,Z为硫元素,W为氯元素。A、同周期元素的从左到右原子半径逐渐减小,则X>Y,Z>W,同主族元素从上到下原子半径逐渐增大,且原子核外电子层数越多,半径越大,则W>X,所以原子半径大小顺序为Z>W>X>Y,故A错误;B、四种元素对应的氢化物分别为NH3、H2O、H2S、HCl,其中NH3的水溶液呈碱性,H2O呈中性,H2S为弱酸,HCl的水溶液为强酸,所以相等物质的量浓度的气态氢化物溶液的pH:X>Y>Z>W,故B正确;C、同周期元素从左到右元素的非金属性逐渐增强,根据元素的非金属性越强,对应最高价氧化物的水化物的酸性越强可知最高价氧化物对应水化物的酸性:W>Z,故D错误;D、四种元素对应的单质中,S在常温下为固体,熔沸点最高,其它元素对应的单质在常温下为气体,故D错误。
考点:位置结构性质的相互关系应用

 名校课堂系列答案
名校课堂系列答案某短周期金属元素原子核外最外层电子数是最内层电子数的1.5倍,下列说法正确的是( )
| A.该元素的单质性质活泼,具有较强的还原性,可以用于某些金属冶炼 |
| B.该元素的单质常温下不与浓硫酸反应 |
| C.该元素的单质无需特别保存,因为其性质稳定,不易与空气中的成分反应 |
| D.该元素的最高价氧化物对应的水化物只能与酸反应 |
下列关于科学家及其提出学说、贡献的叙述错误的是
| A.道尔顿提出原子学说 |
| B.卢瑟福根据α粒子散射现象,提出了带核的原子结构模型 |
| C.汤姆生发现电子,并提出原子结构轨道模型 |
| D.舍勒发现了氯气 |
短周期元素X、Y、Z、W 的原子序数依次增大,且原子最外层电子数之和为13。X 的原子半径比Y 的小,X 与W 同主族,Z 是地壳中含量最高的元素。下列判断合理的是
| A.元素W分别与X、Y、Z形成的化合物都是离子化合物 |
| B.四种元素简单离子的半径:X < Y < Z < W |
| C.Z与其他三种元素形成的常见化合物中有离子晶体、原子晶体和分子晶体 |
| D.只含X、Y、Z 三种元素的化合物,可能是离子化合物,也可能是共价化合物 |
X、Y、Z、W、Q是原子序数依次增大的5种短周期主族元素。其中只有Z是金属,W的单质是黄色固体,X、Y、W在周期表中的相对位置关系如图所示。下列说法正确的是( )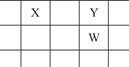
| A.5种元素中,原子半径最大的是W |
| B.Y与Z形成的化合物都可以和盐酸反应 |
| C.Y的简单阴离子比W的简单阴离子还原性强 |
| D.Z与Q形成的化合物水溶液一定显酸性 |
短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示。其中Y所处的周期序数与族序数相等。下列说法正确的是( )
| | | X | |
| Y | Z | | W |
A.原子半径:Y<Z<W
B.气态氢化物的稳定性:X>Z
C.最高价氧化物对应水化物的酸性:Z>W
D.W的最高价氧化物与水反应形成的化合物是离子化合物
X、Y均为短周期元素,X位于ⅠA族,X、Y能形成X2Y型化合物,下列说法中正确的是( )
| A.X与Y形成的化合物中原子个数比可能为1∶1 |
| B.X2Y不可能是共价化合物 |
| C.X和Y分别形成的简单离子不可能具有相同电子层结构 |
| D.根据周期表递变规律判断X原子半径一定大于Y原子半径 |
