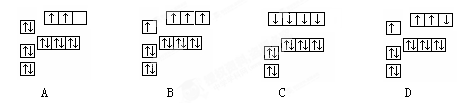
下列各组物质中,互为同位素的是
A.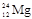 和 和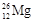 | B.O2和O3 | C.NO和NO2 | D.H2O和H2O2 |
下列关于元素周期表和元素周期律的说法错误的是
| A.Li、Na、K元素的原子核外电子层数随着核电荷数的增加而增多 |
| B.第二周期元素从Li到F,非金属性逐渐增强 |
| C.因为Na比K容易失去电子,所以Na比K的还原性强 |
| D.O与S为同主族元素,且O比S的非金属性强 |
短周期元素X、Y、Z、W在周期表中的相对位置如图,W原子的最外层电子数是其最内层电子数的3倍。下列判断正确的是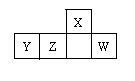
| A.原子半径:X>Y>Z>W |
| B.含Y元素的盐溶液有的显酸性,有的显碱性 |
| C.最简单气态氢化物的热稳定性:Z >W |
| D.X的氢化物能与其最高价氧化物对应的水化物反应生成盐 |
短周期元素X、Y、Z、W、R的原子序数依次增大,X单质在暗处与H2剧烈化合并发生爆炸,Y位于第IA族,Z所处的周期序数与族序数相等,W元素最高正价与最低负价之和为0,R与X同族,则
| A.原子半径:Z>Y>X |
| B.X与R的核电荷数相差18 |
| C.气态氢化物稳定性:W>R |
| D.Y与Z两者最高价氧化物对应的水化物能相互反应 |
已知短周期元素甲、乙、丙、丁、戊的原子序数依次增大,其氢化物中甲、乙、丙、丁、戊的化合价如下,下列说法不正确的是
| 元素 | 甲 | 乙 | 丙 | 丁 | 戊 |
| 化合价 | -3 | -2 | +1 | -4 | -1 |
A.丙的常见氧化物有两种
B.气态氢化物稳定性:甲>乙
C.丁的氧化物能与戊的氢化物的水溶液反应
D.原子半径大小:甲<丙
某元素的原子最外电子层排布是5s25p1,该元素或其化合物不可能具有的性质是 ( )
| A.该元素单质是导体 |
| B.该元素单质在一定条件下能与盐酸反应 |
| C.该元素的最高化合价呈+5价 |
| D.该元素的氧化物的水合物显碱性 |
对充有氖气的霓虹灯管通电,灯管发出红色光。产生这一现象的主要原因( )
| A.在电流的作用下,氖原子与构成灯管的物质发生反应 |
| B.电子由基态向激发态跃迁时吸收除红光以外的光线 |
| C.氖原子获得电子后转变成发出红光的物质 |
| D.电子由激发态向基态跃迁时以光的形式释放能量 |
下列有关物质性质的比较顺序中,不正确的是 ( )
| A.微粒半径:K+>Na+>Mg2+>Al3+ |
| B.热稳定性:HF<HCl<HBr<HI |
| C.酸性:HClO4>H2SO4>H3PO4>H2SiO3 |
| D.熔点:Li>Na>K>Rb |
以下各分子中,所有原子都满足最外层为8电子结构的是 ( )
| A.H3O+ | B.BF3 | C.PCl5 | D.P4O6 |