x、y、z三种短周期元素的原子半径依次变小,原子序数之和为16;这三种元素形成的常见单质分别为X、Y、Z,它们在适当条件下可发生如下图所示转化关系;其中乙和丙均为10电子气体分子,且二者相遇生成弱碱。下列说法正确的是( )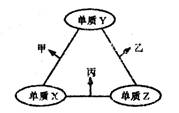
| A.X元素位于第ⅣA族 |
| B.热稳定性:乙<丙 |
| C.甲和丙可能发生氧化还原反应 |
| D.分子乙中各原子均达8电子稳定结构 |
下列说法正确的是
| A.某粒子的电子数等于质子数,则该粒子可能是一种分子或一种离子 |
| B.构成单质的分子中一定含有共价键 |
| C.溶液和胶体的本质区别是有无丁达尔效应 |
| D.化学变化不产生新元素,产生新元素的变化不是化学变化 |
下列物质的性质比较,正确的是
| A.酸性:H2SO4>HClO4>HBrO4 | B.碱性:NaOH>KOH>RbOH |
| C.非金属性: P>S>Cl | D.气态氢化物稳定性:HF>H2O>PH3 |
同主族两种元素原子的核外电子数的差值可能是
| A.6 | B.12 | C.26 | D.30 |
核电荷数小于l8的某元素X,其原子的电子层数为n,最外层电子数为(2n+1),原子核内质子数为(2n2-1)。下列关于元素X的说法中,不正确的是
| A.其最高化合价为+3 | B.可以形成化学式为KXO3的盐 |
| C.其氢化物可以用来做喷泉实验 | D.其最高价氧化物的水化物是强酸 |
短周期元素 X 和 Y 可以形成 XY4型化合物, 若 X 的原子序数为 m , Y 的原子序数为 n , 则 m 和n 的相互关系不可能为
| A.m – 13 = n | B.n + 5 = m | C.m + 8 = n | D.n – 11 =" m" |
据报道,某些建筑材料会产生放射性同位素氡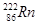 ,从而对人体产生危害。该同位素原子的中子数和质子数之差为
,从而对人体产生危害。该同位素原子的中子数和质子数之差为
| A.136 | B.50 | C.86 | D.222 |
J、Q、M、R、T是原子序数依次增大的短周期主族元素,J、Q、R在周期表中的相对位置如下表。已知J元素最低负化合价的绝对值与其原子最外层电子数相等;M是地壳中含量最多的金属元素。下列说法正确的是
| J | | Q |
| | | R |
A. J和氢元素形成的化合物分子中只含极性共价键
B. R、Q两元素形成的氢化物中,R的氢化物沸点更高
C. J、M、R、T元素最高价氧化物对应的水化物中酸性最强的是H2RO4
D. M单质能与氢氧化钠溶液反应,其中水和氢氧化钠都是氧化剂
元素周期表和元素周期律可以指导人们进行规律性的推测和判断。下列说法不合理的是
| A.微粒X2-与Y2+核外电子排布相同,离子半径:X2-> Y2+ |
| B.人们可在周期表的过渡元素中寻找催化剂、耐腐蚀和耐高温的合金材料 |
| C.由水溶液的酸性:HCl>HF,可推断出元素的非金属性:Cl>F |
| D.Be元素与Al元素同处在周期表的金属与非金属的交界处,可推出: |
已知x、Y是元素周期表中前20号元素,二者原子序数相差3,x、Y能形成化台物M,下列说法正确的是
| A.若X和Y处于同一周期,则X的原子半径肯定小于Y的原子半径 |
| B.若X和Y处于不同的周期,则M溶于水所得溶液肯定呈碱性 |
| C.若M属于离子化合物,则该化合物中只存在离子键 |
| D.若M属于离子化台物,则该化合物中原子个数比可能为1:2 |