下列递变规律正确的是
| A.HClO4、H2SO4、H3PO4的酸性依次增强 |
| B.HCl、HBr 、HI的稳定性依次增强 |
| C.钠、镁、铝的还原性依次减弱 |
| D.N、O、F原子半径逐渐增大 |
两种微粒含有相同的质子数和电子数,这两种微粒可能是
①两种不同的原子;②两种不同元素的原子;③一种原子和一种分子;④一种原子和一种离子;⑤两种不同分子;⑥一种分子和一种离子;⑦两种不同阳离子;⑧两种不同阴离子;⑨一种阴离子和一种阳离子
| A.①③⑤⑥⑦⑧ | B.①③⑤⑦⑧ |
| C.①③④⑤⑦ | D.全部都是 |
X、Y代表两种非金属元素,下列不能说明非金属性X比Y强的是( )
| A.Y的阴离子Y—的还原性强于X的阴离子X— |
| B.X的氢化物的水溶液的酸性比Y的氢化物的水溶液的酸性强 |
| C.X的单质X2能将Y的阴离子Y—氧化成Y2 |
| D.X、Y的单质分别与Fe化合,产物中前者Fe为+3价,后者Fe为+2价 |
已知短周期元素的离子:aA2+、bB+、cC3-、dD- 都具有相同的电子层结构,则下列叙述正确的是
| A.离子半径 C>D>B>A | B.原子序数 D>C>B>A |
| C.原子半径 A>B>D>C | D.单质的还原性 A>B>D>C |
下列各分子中,所有原子都满足最外层为8电子结构的是
| A.H2O | B.BF3 | C.CCl4 | D.PCl5 |
决定原子种类的因素是
| A.质子数和中子数 | B.质子数 | C.电子数 | D.质子数和电子数 |
几种短周期元素的原子半径及主要化合价见下表:
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.102 | 0.089 | 0.074 |
| 主要化合价 | +2 | +3 | +6、-2 | +2 | -2 |
A.L、Q形成的简单离子核外电子数相等
B.L、R的单质与盐酸反应速率为R>L
C.Q、T两元素的氢化物的稳定性为HnT<HnQ
D.M与T形成的化合物能与NaOH溶液反应
下表为元素周期表前四周期的一部分,且X、Y、Z、R和W为主族元素。下列说法正确的是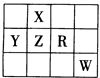
| A.五种元素可能都是金属元素 |
| B.五种元素的原子最外层电子数一定都大于2 |
| C.X的氢化物的沸点一定比Z的氢化物的沸点高 |
| D.R的最高价氧化物对应的水化物一定是强酸 |
X、Y、Z、W均为短周期元素,它们在元素周期表中的位置如图所示。若Y原子的最外层电子数是次外层电子数的3倍,下列说法中正确的是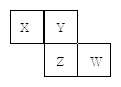
| A.原子半径:W> Z>Y>X |
| B.最高价氧化物对应水化物的酸性:Z>W>X |
| C.4种元素的单质中,Z单质的熔、沸点最低 |
| D.W单质能与水反应,生成一种具有漂白性的物质 |
下列说法正确的是
| A.CO2、CCl4、CH4三个分子中所有原子都满足最外层8电子结构 |
| B.第ⅠA族的金属元素形成的单质的熔点随原子序数的递增而降低 |
| C.第ⅦA族元素形成的单质的熔点随原子序数的递增而降低 |
| D.第ⅠA族元素燃烧形成的氧化物中氧的化合价都不是-2 |