题目内容
X、Y代表两种非金属元素,下列不能说明非金属性X比Y强的是( )
| A.Y的阴离子Y—的还原性强于X的阴离子X— |
| B.X的氢化物的水溶液的酸性比Y的氢化物的水溶液的酸性强 |
| C.X的单质X2能将Y的阴离子Y—氧化成Y2 |
| D.X、Y的单质分别与Fe化合,产物中前者Fe为+3价,后者Fe为+2价 |
B
解析试题分析:A.Y的阴离子Y—的还原性强于X的阴离子X—,则元素的非金属性X比Y强,错误;B.X的氢化物的水溶液的酸性比Y的氢化物的水溶液的酸性强 ,则不能说明元素的非金属性的相对强弱,正确;C.X的单质X2能将Y的阴离子Y—氧化成Y2,则元素的非金属性X强于Y。错误;D.元素的非金属性强的能够把变价金属氧化为高价态,元素的非金属性弱的只能把金属氧化为低价态。因此X、Y的单质分别与Fe化合,产物中前者Fe为+3价,后者Fe为+2价,能够证明元素的非金属性X大于Y。
考点:考查元素的非金属性强弱比较的知识。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
甲—辛等八种元素在周期表中的相对位置如下表。甲与戊的原子序数相差3,戊的一种单质是自然界硬度最大的物质,丁与辛属同周期元素,下列判断不正确的是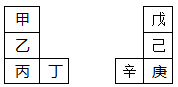
| A.乙的单质在空气中燃烧生成只含离子键的化合物 |
| B.原子半径:辛>己>戊 |
| C.丙与庚的原子核外电子数相差13 |
| D.最高价氧化物的水化物的碱性:丙>乙>甲 |
决定元素种类的因素是( )
| A.核外电子数 | B.最外层电子数 | C.核电荷数 | D.中子数 |
下列各组物质的性质及粒子的性质变化正确的是
| A.稳定性H2S>HCl>HBr>HI | B.酸性HF>HCl>HBr>HI |
| C.离子半径K+>Cl->S2->S | D.酸性HClO4>H2SO4>H2CO3>HClO |
下表为元素周期表前四周期的一部分,且X、Y、Z、R和W为主族元素。下列说法正确的是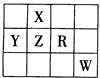
| A.五种元素可能都是金属元素 |
| B.五种元素的原子最外层电子数一定都大于2 |
| C.X的氢化物的沸点一定比Z的氢化物的沸点高 |
| D.R的最高价氧化物对应的水化物一定是强酸 |
元素的以下性质,随着原子序数的递增不呈周期性变化的是
| A.化合价 | B.原子半径 |
| C.相对原子质量 | D.金属性和非金属性 |
短周期元素甲,乙,丙,丁的原子序数依次增大,甲和乙形成的气态化合物的水溶液呈碱性,乙位于第VA族,甲和丙同主族,丁原子最外层电子数和电子层数相等,则 ( )
| A.原子半径 丁 >丙>乙 |
| B.单质的还原性丁>丙>甲 |
| C.甲,乙,丙的氧化物均为共价化和物 |
| D.乙,丙,丁的最高价氧化物对应的水化物能相互反应 |
下列现象和应用与电子跃迁无关的是( )
| A.激光 | B.焰色反应 | C.原子光谱 | D.石墨导电 |
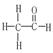 ,其一个分子中存在7对共用电子对
,其一个分子中存在7对共用电子对