题目内容
已知短周期元素的离子:aA2+、bB+、cC3-、dD- 都具有相同的电子层结构,则下列叙述正确的是
| A.离子半径 C>D>B>A | B.原子序数 D>C>B>A |
| C.原子半径 A>B>D>C | D.单质的还原性 A>B>D>C |
A
解析试题分析:A。对于aA2+、bB+、cC3-、dD- 都具有相同的电子层结构,核电荷数越大,离子半径就越小C>D>B>A,正确;B.原子失去电子形成阳离子,原子获得电子形成阴离子,因此原子序数 所以离子半径A>B>D>C,错误;C.同一周期的元素,原子序数越大,原子半径就越小,不同周期的元素,原子核外电子层数越多,原子半径就越大,所以原子半径B> A>C>D,错误;D.同一周期的元素,原子序数越小,元素的金属性就越强。元素的金属性越强,元素单质的还原性就越强,单质的还原性B>A>C>D,错误。
考点:考查相同的电子层结构相同的离子的性质的比较的知识。

练习册系列答案
相关题目
主族元素X、Y、Z的常见离子为aX+、bY2—、cZ—,半径大小关系是X+<Z—<Y2—下列说法不正确的是
| A.b一定小于c | B.单质的氧化性Z > Y |
| C.Y2—的还原性大于Z— | D.X、Y可处于同周期或X在Y的下周期 |
X、Y、Z、W均为短周期元素,它们在元素周期表中的位置如图所示。若Y原子的最外层电子数是次外层电子数的3倍,下列说法中正确的是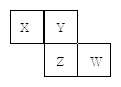
| A.原子半径:W> Z>Y>X |
| B.最高价氧化物对应水化物的酸性:Z>W>X |
| C.4种元素的单质中,Z单质的熔、沸点最低 |
| D.W单质能与水反应,生成一种具有漂白性的物质 |
元素在周期表中的位置,反映了元素的原子结构和元素的性质,下列说法正确的是( )
| A.同一元素不可能既表现金属性,又表现非金属性 |
| B.第三周期元素的最高正化合价等于它所处的主族序数 |
| C.短周期元素原子形成简单离子后,最外层电子都达到8电子稳定结构 |
| D.同一主族的元素的原子,最外层电子数相同,化学性质完全相同 |
核磁共振技术已广泛应用于复杂分子结构的测定和医学诊断等高科技领域。已知只有质子数或中子数为奇数的原子核才有此性质。下列原子可产生核磁共振现象的是
| A.18O | B.28Si | C.32S | D.40K |
列关于同主族元素的说法错误的是( )
| A.同主族元素随原子序数递增,元素原子的得电子能力逐渐增强 |
| B.同主族元素随原子序数递增,单质氧化能力逐渐减弱 |
| C.同主族元素原子最外层电子数都相同 |
| D.同主族元素的原子半径,随原子序数增大而逐渐增大 |
X、Y、Z是原子序数依次增大的短周期主族元素,X2-、Z+都与Mg2+具有相同的核外电子层结构。则下列说法中正确的是
| A.Y元素位于第二周期第ⅦA族或0族 |
| B.X、Y、Z三种元素中非金属性最强的是X元素 |
| C.X、Y、Z三种元素形成的简单离子的半径都比Mg2+半径小 |
| D.Z分别与X、Y形成的化合物都是离子化合物 |