能符合如下图所示的转化关系的元素是 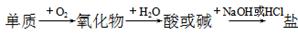
| A.硅 | B.硫 | C.铜 | D.铁 |
下列关于浓硝酸的叙述正确的是
| A.具有挥发性,因而浓硝酸略带有黄色 | B.具有不稳定性,实验室里应保存在棕色瓶中 |
| C.具有强氧化性,常温下可以溶解铝片 | D.具有酸性,实验室可以用它来制氢气 |
(3分)(2012?山东)下列由相关实验现象所推出的结论正确的是( )
| A.Cl2、SO2均能使品红溶液褪色,说明二者均有氧化性 |
| B.向溶液中滴加酸化的Ba(NO3)2溶液出现白色沉淀,说明该溶液中一定有SO2﹣4 |
| C.Fe与稀HNO3、稀H2SO4反应均有气泡产生,说明Fe与两种酸均发生置换反应 |
| D.分别充满HCl、NH3的烧瓶倒置于水中后液面均迅速上升,说明二者均易溶于水 |
下列有关说法不正确的是
| A.实验室制取氢气,为了加快反应速率,可向稀H2SO4中滴加少量Cu(NO3)2溶液 |
| B.为处理锅炉水垢中的CaSO4,可先用饱和Na2CO3溶液浸泡,再加入盐酸溶解 |
C.已知NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l) ΔH=-57.3 kJ·mol-1,则水电离的热化学方程式为:H2O(l) H+(aq)+OH-(aq)ΔH= +57.3 kJ·mol-1 H+(aq)+OH-(aq)ΔH= +57.3 kJ·mol-1 |
| D.生铁发生吸氧腐蚀和析氢腐蚀的负极反应均为:Fe-2e- =Fe2+ |
下列说法正确的是
| A.煤的干馏、石油的分馏都是物理变化 |
| B.工业上常用澄清石灰水和氯气反应制漂白粉 |
| C.蛋白质溶液中加入硫酸铵溶液和硫酸铜溶液均能产生白色沉淀,都属于“盐析” |
| D.二氧化硅可以用于制造光导纤维,光导纤维遇强碱会“断路” |
一定量的锌与100 mL 18.5 mol/L的浓硫酸充分反应后,锌完全溶解,同时生成气体甲 33.6 L(标准状况)。将反应后的溶液稀释至1 L,测得溶液中c(H+)="0.1" mol/L,则下列叙述中错误的是( )
| A.气体甲为SO2和H2的混合物 | B.气体甲中SO2与H2的体积之比为4:1 |
| C.反应中共消耗97.5 g Zn | D.反应中共转移3 mol电子 |
下列关于卤素的叙述,错误的是( )
| A.单质的颜色随核电荷数的增加逐渐加深 |
| B.单质的氧化性随核电荷数的增加而减弱 |
| C.F2通入NaCl水溶液中反应,生成NaF和Cl2 |
| D.可用硝酸酸化的硝酸银溶液来鉴别Cl—、Br— 、I—离子 |
2014年世界环境日中国主题为“向污染宣战”,下列有关环境污染的叙述错误的是( )
| A.大气污染主要指CO、SO2、氮氧化物以及粉尘等 |
| B.氮氧化物是造成光化学烟雾的主要原因 |
| C.臭氧可以杀菌消毒,空气中的臭氧含量越高,对人体健康越有利 |
| D.酸雨通常是指pH在5.6以下的降水 |
将18 g铜和铁的混合物投入200 mL稀硝酸中,充分反应后得到标准状况下2.24 L NO,剩余9.6 g金属;继续加入200 mL等浓度的稀硝酸,金属完全溶解,又得到标准状况下2.24 L NO。若向反应后的溶液中加入KSCN溶液,溶液不变红,则下列说法中正确的是( )
| A.原混合物中铜和铁各0.15 mol | B.稀硝酸的物质的量浓度为1 mol·L-1 |
| C.第一次剩余9.6 g金属为铜和铁 | D.再加入上述200 mL稀硝酸,还会得到标准状况下2.24 L NO |
下列化学实验事实及其结论都正确的是( )
| 选项 | 实验事实 | 结论 |
| A | 将SO2通入含HClO的溶液中生成H2SO4 | HClO的酸性比H2SO4强 |
| B | 铝箔在酒精灯火焰上加热熔化但不滴落 | 铝箔表面氧化铝熔点高于铝 |
| C | 稀、浓硝酸分别与铜反应,还原产物分别为NO和NO2 | 稀硝酸氧化性比浓硝酸强 |
| D | 将SO2通入溴水中,溴水褪色 | SO2具有漂白性 |