题目内容
下列化学实验事实及其结论都正确的是( )
| 选项 | 实验事实 | 结论 |
| A | 将SO2通入含HClO的溶液中生成H2SO4 | HClO的酸性比H2SO4强 |
| B | 铝箔在酒精灯火焰上加热熔化但不滴落 | 铝箔表面氧化铝熔点高于铝 |
| C | 稀、浓硝酸分别与铜反应,还原产物分别为NO和NO2 | 稀硝酸氧化性比浓硝酸强 |
| D | 将SO2通入溴水中,溴水褪色 | SO2具有漂白性 |
B
解析试题分析:A.将SO2通入含HClO的溶液中生成H2SO4, 是因为HClO的氧化性比H2SO4强,能够把SO2氧化为H2SO4。错误。B.铝箔在酒精灯火焰上加热熔化但不滴落,是由于加热时在金属表面产生了熔点高于铝的氧化铝,包裹在熔化的Al的外边,是其不至于滴落。正确。C.稀、浓硝酸分别与铜反应,还原产物分别为NO和NO2,是浓硝酸氧化性比稀硝酸强,它把NO又氧化为NO2。错误。D.将SO2通入溴水中,溴水褪色,是由于发生反应Br2+2H2O+SO2= SO42-+4H++2Br-,这是SO2的还原性。错误。
考点:考查化学所以现象与反应原因的关系的知识。

练习册系列答案
相关题目
下列关于浓硝酸和浓硫酸的叙述,正确的是( )
| A.常温下都能用铝制容器贮存 |
| B.常温下都能与铜较快反应 |
| C.露置在空气中,容器内酸液的质量减轻 |
| D.露置在空气中,容器内酸液的浓度均因吸水而降低 |
下列物质中,属于同素异形体的是
| A.S2和S4 | B.CO和CO2 | C.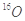 和 和 | D.H2和D2 |
下列说法中正确的是
| A.硅主要以单质、氧化物、硅酸盐的形式存在于自然界中 |
| B.青铜是我国使用最早的合金,钢是用量最大、用途最广泛的合金 |
| C.铁容器可以盛放浓盐酸、浓硝酸、浓硫酸 |
| D.漂白粉、漂粉精可用来漂白棉、麻、纸张,不能用作游泳池及环境的消毒剂 |
次氯酸钠能有效地杀灭水中的细菌和病毒。该过程不可能涉及的变化有
| A.置换反应 | B.复分解反应 | C.电离 | D.水解 |
下列说法正确的是
| A.煤的干馏、石油的分馏都是物理变化 |
| B.工业上常用澄清石灰水和氯气反应制漂白粉 |
| C.蛋白质溶液中加入硫酸铵溶液和硫酸铜溶液均能产生白色沉淀,都属于“盐析” |
| D.二氧化硅可以用于制造光导纤维,光导纤维遇强碱会“断路” |
三氟化氮(NF3)是一种无色无味的气体,它是氨(NH3)和氟(F2)在一定条件下直接反应得到:4NH3+3F2=NF3+3NH4F 。下列有关NF3的叙述正确的是
| A.NF3是离子化合物 | B.NF3分子构型是平面三角形 |
| C.NF3的氧化性比F2强 | D.NF3中的N呈+3价 |
下列两种物质间发生反应,消耗等物质的量的酸,产生气体最多的是
| A.木炭与浓硝酸 | B.铜与稀硝酸 | C.锌与稀硫酸 | D.木炭与浓硫酸 |
化学在生产和日常生活中有着重要的应用。下列叙述正确的是
| A.单质硅是将太阳能转化为电能的常用材料 |
| B.硅酸钠的俗名为玻璃,可用于制备硅胶和木材防火剂 |
| C.用浓H2SO4刻蚀工艺玻璃上的纹饰 |
| D.SO2具有氧化性,可用来漂白纸浆 |