题目内容
下列关于卤素的叙述,错误的是( )
| A.单质的颜色随核电荷数的增加逐渐加深 |
| B.单质的氧化性随核电荷数的增加而减弱 |
| C.F2通入NaCl水溶液中反应,生成NaF和Cl2 |
| D.可用硝酸酸化的硝酸银溶液来鉴别Cl—、Br— 、I—离子 |
C
解析试题分析:A.在卤素单质中,F2是淡黄绿色气体;Cl2是黄绿色气体;Br2是深红棕色液体;I2是紫黑色固体。因此单质的颜色随核电荷数的增加逐渐加深。正确。B.元素的非金属性F>Cl>Br>I,元素的非金属性越强,单质的氧化性就越强,所以卤素单质的氧化性随核电荷数的增加而减弱。正确。C.F2通入NaCl水溶液中发生反应:2F2+2H2O=4HF+O2反应,所以不能生成NaF和Cl2。错误。D.向待测溶液中加入AgNO3溶液,并加入硝酸酸化,若产生白色沉淀,则溶液中含有Cl-;若产生淡黄色沉淀,则含有Br-;若产生黄色沉淀,就证明含有I-。因此可用硝酸酸化的硝酸银溶液来鉴别Cl—、Br— 、I—离子。正确。
考点:考查卤素的单质或化合物的性质及递变规律的知识。

练习册系列答案
相关题目
下列关于硅单质及其化合物的说法正确的是 ①硅是构成一些岩石和矿物的基本元素
①硅是构成一些岩石和矿物的基本元素 ②水泥、玻璃、水晶饰物都是硅酸盐制品
②水泥、玻璃、水晶饰物都是硅酸盐制品 ③高纯度的硅单质广泛用于制作光导纤维
③高纯度的硅单质广泛用于制作光导纤维  ④陶瓷是人类应用很早的硅酸盐材料
④陶瓷是人类应用很早的硅酸盐材料
| A.①② | B.②③ | C.①④ | D.③④ |
在允许加热的条件下,只用一种试剂就可以鉴别硫酸铵、氯化钾、氯化镁、硫酸铝和硫酸铁溶液,这种试剂是( )
| A.NaOH | B.NH3·H2O | C.AgNO3 | D.BaCl2 |
相同质量的铜片分别与过量的体积相同的浓硝酸、稀硝酸反应。二者比较,相等的是
① 铜片消耗完所需时间;② 反应生成的气体体积(标准状况);③ 反应中氧化剂得到的电子总数;④ 反应后溶液中铜离子的浓度
| A.①③ | B.②④ | C.③④ | D.只有① |
下列陈述Ⅰ、Ⅱ均正确且有因果关系的是:( )
| 选项 | 陈述Ⅰ | 陈述Ⅱ |
| A | 动物油脂相对不容易被氧化 | 油脂工业通常要将液态油脂氢化 |
| B | HNO3具有酸的通性 | 硝酸常用作金属铜加工前的酸洗 |
| C | 明矾可以净水 | 浑浊的石灰水加入明矾会变澄清 |
| D | Si是一种非金属单质 | 单质Si能与NaOH溶液反应 |
下列关于浓硝酸的叙述正确的是
| A.具有挥发性,因而浓硝酸略带有黄色 | B.具有不稳定性,实验室里应保存在棕色瓶中 |
| C.具有强氧化性,常温下可以溶解铝片 | D.具有酸性,实验室可以用它来制氢气 |
基于实验现象的推论,你认为合理的是( )
| 选项 | 实验现象 | 推论 |
| A | 乙烯气体可以使溴水褪色 | 乙烯发生取代反应 |
| B | 浓硫酸电导率比较低 | 硫酸浓度大时是弱电解质 |
| C | 氨气用于喷泉实验 | 氨气极易溶于水 |
| D | 硝酸溶液使pH试纸先变红后变白 | 硝酸酸性太强不能用pH试纸检测 |
海水是巨大的资源宝库,下列关于海水综合利用的说法错误的是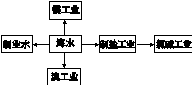
| A.海水制淡水主要有蒸馏法、电渗析法、离子交换法等 |
| B.海水制盐、发展氯碱工业都是发生物理变化 |
| C.海水提溴过程中先通入Cl2将溴离子氧化为溴单质 |
| D.工业上用电解熔融MgCl2的方法制取金属镁 |
实验室制取少量干燥的氨气涉及下列装置,其中正确的是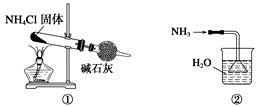
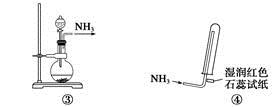
| A.①是氨气发生装置 | B.③是氨气发生装置 |
| C.②是氨气吸收装置 | D.④是氨气收集、检验装置 |