某溶液中含有大量的Cl一、Br一、I一,若向l L该混合溶液中通入一定量的Cl2,溶液中Cl-、Br一、I一的物质的量与通入Cl2的体积(标准状况)的关系如下表所示,原溶液中Cl一、Br一、I一的物质的量浓度之比为( )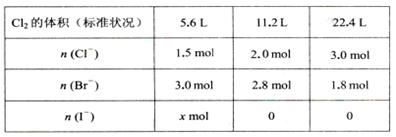
| A.5:15:4 | B.5:12:4 | C.15 : 30 : 8 | D.条件不足,无法计算 |
已知X和Y是两种单质,X+Y→X2++Y2-,现有下列叙述正确的是: ①X被氧化,②X是氧化剂,③Y2-是还原产物,④X2+具有氧化性,⑤Y2-具有还原性,⑥Y单质氧化性比X2+氧化性强( )
| A.①②③ | B.①②⑥ | C.①③④⑤⑥ | D.①③④⑤ |
一定体积的KMnO4溶液恰好能氧化一定质量的KHC2O4·H2C2O4·2H2O。若用0.1000mol/L的NaOH溶液中和相同质量的KHC2O4·H2C2O4·2H2O,所需NaOH溶液的体积恰好为KMnO4溶液的3倍,则KMnO4溶液的浓度(mol/L)为( )
提示:①H2C2O4是二元弱酸
②10[KHC2O4·H2C2O4]+8KMnO4+17H2SO4=8MnSO4+9K2SO4+40CO2↑+32H2O
| A.0.008889 | B.0.08000 | C.0.1200 | D.0.2400 |
对于反应:TiCl4+4Na=4NaCl+Ti,下列说法正确的是
| A.该反应说明钠是强还原剂,可用于冶炼金属 |
| B.该反应条件是TiCl4在熔融状态或水溶液中 |
| C.Ti是氧化剂 |
| D.TiCl4是还原剂 |
下列反应中,水只表现氧化性的是
| A.2Na +2H2O =2NaOH +H2↑ |
| B.Cl2 +H2O =HCl + HClO |
| C.2F2 +2H2O =4HF +O2 |
| D.CaO +H2O =Ca(OH)2 |
为了探究铁及其化合物的氧化性和还原性,某同学设计了如下实验方案,其中符合实验要求且完全正确的是
| | 实验操作 | 实验现象 | 离子反应 | 实验结论 |
| A | 在氯化亚铁溶液中滴加新制氯水 | 浅绿色溶液变成棕黄色溶液 | 2Fe2++Cl2= 2Fe3++2Cl- | Fe2+具有还原性 |
| B | 在氯化亚铁溶液中加入锌片 | 浅绿色溶液变成无色溶液 | Fe2++Zn= Fe+Zn2+ | Zn具有还原性 |
| C | 在氯化铁溶液中加入铁粉 | 棕黄色溶液变成浅绿色溶液 | Fe3++Fe= 2Fe2+ | 铁单质具有还原性 |
| D | 在氯化铁溶液中加入铜粉 | 蓝色溶液变成棕黄色溶液 | 2Fe3++Cu= 2Fe2++Cu2+ | Fe3+具有氧化性 |
下列变化中,属于还原反应的是
| A.Cl-→Cl2 | B.FeCl2→FeCl3 | C.C→CO2 | D.KMnO4→MnO2 |
下列变化需要加入适当的氧化剂才能实现的是
A.CuO Cu Cu | B.Fe2+ Fe Fe | C.H2SO4 SO2 SO2 | D.HCl Cl2 Cl2 |
三氟化氮(NF3)是一种新型电子材料,它在潮湿的空气中与水蒸气能发生氧化还原反应,其反应的产物有:HF、NO和HNO3。则下列说法正确的是
| A.反应过程中,被氧化与被还原的元素的物质的量之比为2:1 |
| B.NF3是一种无色、无臭的气体,因此NF3在空气中泄漏时不易被察觉 |
| C.一旦NF3泄漏,可以用石灰水溶液喷淋的方法减少污染 |
| D.若反应中转移的电子数目为6.02×1023,生成22.4L NO气体 |
在AlCl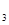 和FeCl
和FeCl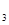 混合溶液中,先加入过量的KI溶液,再加入足量的Na
混合溶液中,先加入过量的KI溶液,再加入足量的Na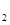 S溶液,所得 到的沉淀物是
S溶液,所得 到的沉淀物是
A.Fe(OH)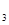 、Al(OH) 、Al(OH)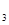 | B.Al(OH)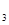 、I 、I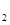 |
C.Fe S S 、I 、I | D.FeS、S、Al(OH) |