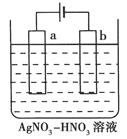
a mol FeS与b mol Fe3O4投入到V L c mol·L-1的硝酸溶液中恰好完全反应,假设只产生NO气体。所得澄清溶液的成分是Fe(NO3)3和H2SO4的混合液,则反应中未被还原的硝酸为( )
| A.(a+3b) mol | B.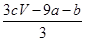 mol mol |
C.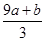 mol mol | D.(cV-3a-9b) mol |
ClO2是一种杀菌消毒效率高的水处理剂,实验室可通过以下反应制得:2KClO3+H2C2O4+H2SO4=2ClO2↑+K2SO4+2CO2↑+2H2O。下列说法中不正确的是( )
| A.ClO2是还原产物 |
| B.1 mol KClO3参加反应,失去电子为1 mol |
| C.H2C2O4在反应中被氧化 |
| D.H2C2O4的还原性大于ClO2的还原性 |
下列反应中,氧化剂与还原剂的物质的量之比为1:2的是
①O3+2KI+H2O=2KOH+I2+O2 ②SiO2+2C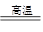 Si+2CO↑
Si+2CO↑
③SiO2+3C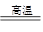 SiC+2CO↑ ④4HCl(浓)+MnO2
SiC+2CO↑ ④4HCl(浓)+MnO2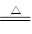 MnCl2+Cl2↑+2H2O( )
MnCl2+Cl2↑+2H2O( )
| A.仅有② | B.②④ | C.②③④ | D.①②③④ |
LiAlH4是重要的储氢材料,其组成类似于Na3AlF6。常见的供氢原理如下面两个方程式所示:
①2LiAlH4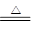 2LiH+2Al+3H2↑
2LiH+2Al+3H2↑
②LiAlH4+2H2O=LiAlO2+4H2↑
下列说法正确的是( )
| A.LiAlH4是共价化合物,LiH是离子化合物 |
| B.生成等质量的氢气,反应①、②转移电子数之比为4?3 |
| C.氢化锂也是一种储氢材料,供氢原理为LiH+H2O=LiOH+H2↑ |
| D.若反应①中生成3.36 L氢气,则一定有2.7 g铝生成 |
将51.2 g Cu完全溶于适量浓硝酸中,收集到氮的氧化物(含NO、N2O4、NO2)的混合物,这些气体恰好能被500 mL 2.0 mol/L NaOH溶液完全吸收,生成含NaNO3和NaNO2的盐溶液,其中NaNO3的物质的量是( )
| A.0.2 mol | B.0.4 mol | C.0.6 mol | D.0.8 mol |
已知:
①向KMnO4晶体中滴加浓盐酸,产生某黄绿色气体;
②向FeCl2溶液中通入少量实验①产生的气体,溶液变黄色;③取实验②生成的溶液滴在淀粉KI试纸上,试纸变蓝色。
下列判断中正确的是( )
| A.①中产生气体的电子式是Cl?Cl |
| B.上述实验中,共有两个氧化还原反应 |
| C.实验②中FeCl2被氧化 |
| D.实验③发生的是同主族元素单质间的置换反应 |
以下有关实验原理及结论正确的是( )
| A.XCl3的溶液能与铜片发生反应,则铜的金属性一定比X强 |
| B.金属X能与NaOH溶液反应放出H2,但金属Y不能,则Y的金属性一定比X弱 |
| C.非金属X能将Fe氧化到+3价,但非金属Y不能,则Y的氧化性一定比X强 |
| D.Na2SO3溶液使酸性KMnO4溶液褪色:5SO32—+6H++2MnO4—=5SO42—+2Mn2++3H2O |
在Cu2S+2Cu2O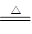 6Cu+SO2↑反应中,说法正确的是( )
6Cu+SO2↑反应中,说法正确的是( )
| A.Cu2O在反应中被氧化 |
| B.Cu2S在反应中既是氧化剂又是还原剂 |
| C.Cu既是氧化产物又是还原产物 |
| D.若反应中转移12 mol电子,则生成6 mol Cu |
下列变化中,必须加入还原剂才能发生的是
| A.FeCl2→FeCl3 | B.H2O→H2 | C.Al→NaAlO2 | D.CO2→C |