题目内容
a mol FeS与b mol Fe3O4投入到V L c mol·L-1的硝酸溶液中恰好完全反应,假设只产生NO气体。所得澄清溶液的成分是Fe(NO3)3和H2SO4的混合液,则反应中未被还原的硝酸为( )
| A.(a+3b) mol | B.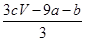 mol mol |
C.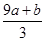 mol mol | D.(cV-3a-9b) mol |
B
解析

练习册系列答案
相关题目
下列反应属于氧化还原反应,但水既没有做氧化剂又没有做还原剂的是
| A.2F2+2H2O ="4HF" +O2 |
| B.Na2O+H2O=2NaOH |
| C.Cl2+H2O =2HCl+HClO |
| D.CaO+H2O =Ca(OH)2 |
下列实验的现象与对应的结论均正确的是
| 选项 | 操 作 | 现 象 | 结 论 |
| A | 向溶液X中滴加NaOH稀溶液,将湿润的红色石蕊试纸置于试管口 | 试纸不变蓝 | 溶液X中无NH |
| B | 将少量的溴水滴入FeCl2、NaI的混合溶液中,再滴加CCl4,振荡、静置,向上层溶液中滴加KSCN溶液 | 上层溶液不变红, 下层溶液紫红色 | 氧化性:Br2>Fe3+>I2 |
| C | 将水蒸气通过灼热的铁粉 | 粉末变红 | 铁与水在高温下发生反应 |
| D | 向漂白粉上加入较浓的盐酸,将湿润淀粉碘化钾试纸置于试管口 | 产生气泡,试纸未变蓝 | 漂白粉已经失效 |
现有稀硫酸和稀硝酸的混合溶液,已知其中稀硫酸浓度为4mol/L,稀硝酸的浓度为2mol/L。取10mL混合酸,向其中加入过量铁粉,反应结束后,在标准状况下可收集到气体体积为(假设HNO3只被还原为NO)
| A.0.224L | B.0.448L | C.0.672L | D.0.896L |
将51.2 g Cu完全溶于适量浓硝酸中,收集到氮的氧化物(含NO、N2O4、NO2)的混合物,这些气体恰好能被500 mL 2.0 mol/L NaOH溶液完全吸收,生成含NaNO3和NaNO2的盐溶液,其中NaNO3的物质的量是( )
| A.0.2 mol | B.0.4 mol | C.0.6 mol | D.0.8 mol |
向酸化过的MnSO4溶液中滴加(NH4)2S2O8(过二硫酸铵)溶液会发生反应:Mn2++S2O82-+H2O―→MnO4-+H++SO42-。下列说法不正确的是( )
| A.可以利用该反应检验Mn2+ |
| B.氧化性比较:S2O82->MnO4- |
| C.MnSO4溶液可以使用盐酸酸化 |
| D.若有0.1 mol氧化产物生成,则转移电子0.5 mol |
工业上可用硫酸铝与硫磺焙烧制备氧化铝:2Al2(SO4)3+3S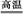 2Al2O3+9SO2↑,下列有关说法中正确的是( )
2Al2O3+9SO2↑,下列有关说法中正确的是( )
| A.反应中Al2(SO4)3被氧化 |
| B.Al2 (SO4)3、Al2O3均含有离子键和共价键 |
| C.5.1 g Al2O3含有9.03×1022个阴离子 |
| D.该反应中,每转移0.3 mol电子生成5.04 L SO2 |
下列工业生产的反应原理不涉及氧化还原反应的是( )
| A.钢铁厂高炉炼铁 |
| B.工业上以氨气为原料用氨碱法生产纯碱 |
| C.硝酸厂以氨气为原料制取硝酸 |
| D.氯碱厂利用氯化钠生产氯气和烧碱 |
京沪高铁铺设的铁轨为稀土钢轨。稀土铈(Ce)元素主要存在于独居石中,金属铈在空气中易氧化变暗,受热时燃烧,遇水很快反应并产生气体。已知:铈常见的化合价为+3和+4,且Ce4++Fe2+=Ce3++Fe3+。下列说法正确的是( )。
| A.用惰性电极电解Ce(SO4)2溶液,可在阴极获得铈 |
| B.将少量的碘化亚铁溶液滴加到Ce(SO4)2溶液中,其离子方程式为Ce4++Fe2+=Ce3++Fe3+ |
| C.金属铈着火时,可用沙土盖灭 |
| D.金属铈可浸于煤油中保存,储存在阴凉、通风的地方,要远离火种和热源 |