将pH=1的稀硫酸慢慢加入—定量的BaCl2的溶液中,恰好使Ba2+沉淀完全,此时溶液的体积为100 mL(混合时溶液体积的变化忽略不计),且混合溶液的pH=2,则原BaCl2溶液中Cl-的浓度约为
| A.0.011 mol/L | B.0.22 mol/L | C.0.022 mol/L | D.0.11 mol/L |
用pH大小表示溶液的酸碱性相对强弱有许多不足之处。因此,荷兰科学家Henk Van Lubeck引入了酸度(AG)的概念,即把电解质溶液中的酸度定义为c(H+)与c(OH一)比值的对数,用公式表示为AG="lg" [c(H+)/c(OH一)] 。常温下,在AG=10的溶液中能大量共存的离子是:
| A.Ca2+、K+、Cl-、SO32- | B.NH4+、Fe2+、 I一、SO42- |
| C.Na+ 、K+、ClO-、S2- | D.Na+、S2O32-、AlO2—、K+ |
对于某酸性溶液(可能含有Br –、SO42 –、H2SO3、NH4+),分别进行如下实验: ①加热时放出的气体可使品红溶液褪色;②加入碱溶液使溶液呈碱性,再加热时放出的气体可使湿润的红色石蕊试纸变蓝;③加入氯水时,溶液略呈橙红色,再加入BaCl2溶液,产生不溶于稀硝酸的白色沉淀。对于下列物质不能确定其在原溶液中是否存在的是
| A.Br – | B.SO42– | C.H2SO3 | D.NH4+ |
某无色透明溶液能与铝粉反应放出H2,则此溶液中一定能大量共存的离子组为
| A.OH-、Na+、K+、MnO4- | B.H+、Cl-、Ba2+、NO3- |
| C.K+、Cl-、Na+、SO42- | D.NH4+、Mg2+、Cl-、HCO3- |
将溶液(或气体)X逐渐加入(或通入)到一定量Y溶液中,产生沉淀的质量与加入X的物质的量关系如下图,符合图中情况的一组物质是 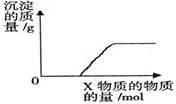
| | (A) | (B) | (C) | (D) |
| X | Ba(HCO3)2 溶液 | Na2CO3 溶液 | KOH 溶液 | CO2 气体 |
| Y | NaOH 溶液 | CaCl2 溶液 | Mg(HSO4)2 溶液 | 石灰水 |
常温下,下列各组离子在指定溶液中一定能大量共存的是
| A.加入Mg能放出H2的溶液:Na+、Al3+、Cl-、SO42- |
| B.常温下,c(H+)/c(OH-)=1010的溶液:Fe2+、K+、NO3-、SO42- |
| C.加入苯酚显紫色的溶液:NH4+、K+、Cl-、S2- |
| D.使甲基橙呈红色的溶液:NH4+、Na+、AlO2-、HCO3- |
下列离子方程式中正确的是
| A.在少量Mg(OH)2悬浊液中滴加氯化铵浓溶液:Mg(OH)2+2NH4+=2NH3·H2O+Mg2+ |
| B.双氧水中滴加2滴FeCl3溶液:Fe3++H2O2=Fe2++O2↑+2H+ |
| C.双氧水加入稀硫酸和KI溶液: H2O2+2H++2I—= I2+ O2↑+2 H2O |
| D.向银氨溶液中加入盐酸:[Ag(NH3)2]++OH﹣+3H+=Ag++2NH4++H2O |
下列离子或分子组中大量共存且满足相应要求的是( )
| A.K+、AlO2-、Cl-、MnO4-要求:无色澄清溶液 |
| B.Fe3+、NO3-、I-、HCO3-要求:逐滴滴加盐酸立即产生气体 |
| C.Na+、K+、Ag+,NO3-要求:逐滴滴加氨水先有沉淀产生,后沉淀消失 |
| D.NH4+、Al3+、SO42-、CH3COOH要求:滴加NaOH浓溶液立刻产生气体 |
在混合体系中,确认化学反应先后顺序有利于问题的解决,下列反应先后顺序判断正确的是
| A.在含等物质的量的FeBr2、FeI2的溶液中缓慢通入Cl2:I-、Br-、Fe2+ |
| B.在含等物质的量的Fe3+、Cu2+、H+的溶液中加入Zn:Fe3+、Cu2+、H+、Fe2+ |
| C.在含等物质的量的Ba(OH)2、KOH的溶液中通入CO2:KOH、Ba(OH)2、BaCO3、K2CO3 |
| D.在含等物质的量的AlO2-、OH-、CO32-溶液中,逐滴加入盐酸:AlO2-、Al(OH)3、OH-、CO32- |