0 96092 96100 96106 96110 96116 96118 96122 96128 96130 96136 96142 96146 96148 96152 96158 96160 96166 96170 96172 96176 96178 96182 96184 96186 96187 96188 96190 96191 96192 96194 96196 96200 96202 96206 96208 96212 96218 96220 96226 96230 96232 96236 96242 96248 96250 96256 96260 96262 96268 96272 96278 96286 203614

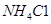 溶液和
溶液和 溶液(中性)。请结合平衡原理和必要的文字解释滤渣C能溶于3mol/L的
溶液(中性)。请结合平衡原理和必要的文字解释滤渣C能溶于3mol/L的