实验室需配制一种c (H+)=2mol/L的强酸溶液500mL,下列配制方法可行的是( )
| A.取100mL5mol/LH2SO4,加入400mL水 |
| B.取200mL5mol/LHCl,加水稀释至500mL |
| C.取200 mL5mol/LH2SO4,加水稀释至500mL |
| D.取100 mL5mol/LHNO3,加水稀释至500mL |
用NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A.2.4g镁原子变成离子时,失去的电子数为0.3NA |
| B.常温常压下,28g氮气所含的原子数为2 NA |
| C.22.4L甲烷(CH4)所含的原子数为5NA |
| D.物质的量浓度为0.5mol / L的MgCl2溶液中,含有Cl—个数为1 NA |
在Na2SO4、NaCl、NaOH的混合溶液中,Na+、SO42-、OH-的个数比是8:1:2,则溶液中Na2SO4、NaCl、NaOH的物质的量之比是
| A.1:1:1 | B.1:4:2 | C.1:2:4 | D.1:3:2 |
| | X | Y | Z |
| A | 氧化物 | 化合物 | 纯净物 |
| B | 胶体 | 分散系 | 混合物 |
| C | 电解质 | 酸、碱、盐 | 化合物 |
| D | 碱性氧化物 | 金属氧化物 | 氧化物 |
下列叙述正确的是( )
| A.0.012 kg12C含有6.02×1023个碳原子 | B.1mol任何物质都含有6.02×1023个原子 |
| C.硫酸的摩尔质量是98g | D.常温常压下,1 mol氧气的体积为22.4L |
把VL含有MgSO4和K2SO4的混合溶液分成两等份,一份加入含a mol BaCl2的溶液,恰好使硫酸根离子完全沉淀为硫酸钡;另一份加入含b mol NaOH的溶液,恰好使镁离子完全沉淀为氢氧化镁。则原混合溶液中钾离子的浓度为
A.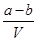 mol·L-1 mol·L-1 | B.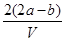 mol·L-1 mol·L-1 |
C. mol·L-1 mol·L-1 | D.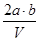 mol·L-1 mol·L-1 |
如图是某学校实验室从化学试剂商店买圆的硫酸试剂标签上的部分内容,据此判断下列说法错误的是
| A.该硫酸具有强烈的腐蚀性,应放于危险化学用品柜中妥善保管 |
| B.取10 mL该硫酸于烧杯中,再加18.4 mL的水,可配得49%的硫酸 |
| C.配制200 mL4.6 mol/L的稀硫酸需取该硫酸50 mL |
| D.该硫酸与等质量的水混合所得溶液的物质的量浓度小于9.2 mol/L |
向100 mL18 mol·L-1 H2SO4溶液中加入足量的铁片加热。充分反应后,产生的气体在标准状况下的体积为
[提示:2Fe+6H2SO4(浓)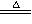 Fe2(SO4)3+3SO2↑+6H2O]
Fe2(SO4)3+3SO2↑+6H2O]
| A.小于20.16 L |
| B.等于20.16 L |
| C.介于20.16 L和40.32 L之间 |
| D.等于40.32 L |
用NA表示阿伏加德罗常数的值。下列叙述中不正确的是
| A.16.9 g过氧化钡(BaO2)固体中阴、阳离子总数约为0.2 NA |
| B.常温常压下,28 g乙烯和环丁烷(C4H8)的混合气体中含有的碳原子数为2 NA |
C.a g某气体含分子数为b,c g该气体在标况下的体积为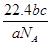 L L |
| D.某密闭容器盛有0.1 molN2和0.3 molH2,在一定条件下充分反应,转移电子的数目为0.6 NA |
设NA为阿伏加德罗常数的数值,下列说法正确的是
| A.25℃时,pH=13的NaOH溶液中含有OH-的数目为0.1NA |
| B.常温常压下, 14 g由N2与CO组成的混合气体含有的原子数目为NA |
| C.0.1L l mol·L-1Na2CO3溶液中,阴离子总数小于0.1NA |
| D.50ml、l8.4 mol/L浓硫酸与足量铜微热反应,生成SO2分子的数目为0.46NA |