题目内容
下列叙述正确的是( )
| A.0.012 kg12C含有6.02×1023个碳原子 | B.1mol任何物质都含有6.02×1023个原子 |
| C.硫酸的摩尔质量是98g | D.常温常压下,1 mol氧气的体积为22.4L |
A
解析试题分析:A.0.012 kg12C含有6.02×1023个碳原子,正确;B. 1 mol任何物质都含有6.02×1023个分子,错误;C.硫酸的摩尔质量是98g/mol,错误; D.标准状况下,1 mol氧气的体积为22.4L,错误。
考点:

练习册系列答案
 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案
相关题目
用NA表示阿伏加德罗常数的值,下列说法中正确的是
| A.1 mol N2所含有的原子数为NA |
| B.标准状况下,22.4 L水中含有的水分子数为NA |
| C.500 mL 1.0 mol/L碳酸钠溶液中所含钠离子的数为NA |
| D.0.5mol纯硫酸所含有的氧原子数与2NA个CO2分子中所含有的氧原子数相等 |
设NA为阿伏加德罗常数的值,下列叙述中正确的是
| A.1mol丙烷分子中,含有的非极性共价键数目为NA |
| B.标准状况下,1.8gH2O分子中所含有的电子数为NA |
| C.25℃时,pH=13的 Ba(OH)2溶液中含有的OH-数目为0.1 NA |
| D.2.24L氯气与过量的氢氧化钠溶液完全反应转移的电子数为0.1NA |
用NA表示阿伏加德罗常数的值。下列叙述中不正确的是
| A.16.9 g过氧化钡(BaO2)固体中阴、阳离子总数约为0.2 NA |
| B.常温常压下,28 g乙烯和环丁烷(C4H8)的混合气体中含有的碳原子数为2 NA |
C.a g某气体含分子数为b,c g该气体在标况下的体积为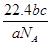 L L |
| D.某密闭容器盛有0.1 molN2和0.3 molH2,在一定条件下充分反应,转移电子的数目为0.6 NA |
以“物质的量”为中心的计算是化学计算的基础,下列与“物质的量”相关的计算正确的( )
| A.现有CO、CO2、O3三种气体,它们分别都含有1molO,则三种气体的物质的量之比为 3∶2∶1 |
| B.5.6g CO 和22.4L CO2中含有的碳原子数一定相等 |
| C.标准状况下,11.2 L X气体分子的质量为16 g,则X气体的摩尔质量是32 |
| D.n g Cl2中有m个Cl原子,则阿伏加德罗常数NA的数值可表示为 35.5m/n |
设NA代表阿伏加德罗常数,下列叙述正确的是 ( )
| A.标准状况下2.24 L H2O中,分子数为0.1NA |
| B.将1mol Cl2通入到水中,则N(HClO)+ N(Cl?)+ N(ClO-)= 2NA |
| C.常温常压下16g O2和O3混合气体中,氧原子数为NA |
| D.7.8g Na2O2与足量水反应,转移电子数为0.2NA |
设法把NO2和O2按4:1体积比充满一干燥的真空烧瓶中,然后把烧瓶置于水中,瓶内液面会逐渐上升,则最终烧瓶中所得溶液的物质的量浓度为(①气体体积为标准状况下测定 ②烧瓶中溶液不向外扩散)( )
| A.1/14mol/L | B.1/22.4mol/L | C.1/28mol/L | D.1/42mol/L |
将23g Na和24g Mg分别投入等质量的过量的盐酸中,反应完毕后,所得溶液的质量分数分别为m和n,则m和n的关系是
| A.m>n | B.m=n | C.m<n | D.无法确定 |
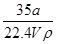 ×100% ②C=
×100% ②C=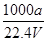 ③上述溶液中再加入VmL水后,所得溶液的质量分数大
③上述溶液中再加入VmL水后,所得溶液的质量分数大