M(NO3)2热分解化学方程式为:2M(NO3)2 2MO+4NO2↑+O2↑,加热29.6g M(NO3)2使其完全分解,在标准状况下收集11.2L的气体,那么M的摩尔质量是
2MO+4NO2↑+O2↑,加热29.6g M(NO3)2使其完全分解,在标准状况下收集11.2L的气体,那么M的摩尔质量是
| A.24g/mol | B.74g/mol | C.148g/mol | D.40g/mol |
同温同压下,等质量的O2和O3相比较,下列结论正确的是
| A.它们的分子数目之比是 1∶1 | B.它们的密度之比为 2∶3 |
| C.它们的体积之比是 1∶1 | D.它们的氧原子数目之比为 2∶3 |
配制250 mL 0.5 mol·L-1的NaOH溶液,在下列仪器中:①量筒 ②250 mL容量瓶 ③托盘天平和砝码 ④500 mL容量瓶 ⑤烧杯 ⑥玻璃棒 ⑦漏斗 ⑧药匙 ⑨胶头滴管
⑩250 mL的烧瓶,需要用到的仪器按使用先后顺序排列正确的是
| A.⑧③⑤⑥②⑨ | B.②③⑦⑤⑥ |
| C.②⑤⑦⑥① | D.④③⑦⑤⑥ |
下列叙述正确的是(NA为阿伏加德罗常数的值)
| A.1 mol Na2O·SiO2中含有NA个Na2O |
| B.在H2O2+Cl2=2HCl+O2反应中,每生成32 g氧气,则转移NA个电子 |
| C.标准状况下,分子数为NA的CO、C2H4混合气体体积约22.4 L,质量为28 g |
| D.4.6 g Na与适量氧气完全反应生成Na2O、Na2O2的混合物中含有的阴离子数大于0.1NA |
配制一定物质的量浓度的NaOH溶液时,使所配制的溶液浓度偏小的操作是
①烧杯中NaOH溶液移入容量瓶后没有洗涤烧杯
②定容后摇匀,发现液面低于刻度线,再滴加蒸馏水至刻度线
③实验用的容量瓶洗净后未干燥,里面含有少量水
④定容时俯视
| A.①② | B.③④ | C.①③ | D.②④ |
设NA为阿伏加德罗常数,下列叙述正确的是
| A.2.4g Mg与足量的二氧化碳完全反应失去的电子数为0.2NA |
| B.22.4 L氯气与过量的铁完全反应,转移电子数为2 NA |
| C.含NA个氧原子的O2与含NA个氧原子的O3的质量之比为2︰3 |
| D.1.8g1H218O中含有的中子数为NA |
物质的量浓度相同的NaCl、MgCl2、AlCl3三种溶液的体积比为3:2:1时,三种溶液中c(Cl-)之比为
| A.1:1:1 | B.3:2:1 | C.1:2:3 | D.3:4:3 |
下列叙述正确的是
| A.1 mol H2O的质量为18g·mol-1 |
| B.质量数为37的氯原子 17 37Cl |
| C.3.01×1023个SO2分子的质量为32g |
| D.标准状况下,1 mol任何物质体积均为22.4L |
某固体A在一定条件下加热分解,产物全是气体,A的分解反应为:2A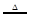 B+2C+2D,现测得分解产生的混合气体对氢气的相对密度为d,则A的相对分子质量为
B+2C+2D,现测得分解产生的混合气体对氢气的相对密度为d,则A的相对分子质量为
| A.2d | B.10d | C.5d | D.0.8d |
科学家刚刚发现了某种元素的原子,1个该原子质量是a g,一个12C的原子质量是b g,NA是阿伏加德罗常数的值,下列说法正确的是
①该原子的相对原子质量为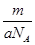
②m g该原子的物质的量为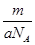 mol
mol
③该原子的摩尔质量是aNA g
④Wg该原子中含有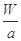 个该原子
个该原子
⑤由已知信息可得: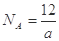
| A.①②④ | B.②③④ | C.①②⑤ | D.①③⑤ |