题目内容
下列叙述正确的是(NA为阿伏加德罗常数的值)
| A.1 mol Na2O·SiO2中含有NA个Na2O |
| B.在H2O2+Cl2=2HCl+O2反应中,每生成32 g氧气,则转移NA个电子 |
| C.标准状况下,分子数为NA的CO、C2H4混合气体体积约22.4 L,质量为28 g |
| D.4.6 g Na与适量氧气完全反应生成Na2O、Na2O2的混合物中含有的阴离子数大于0.1NA |
C
解析试题分析:A、Na2O·SiO2中不含Na2O,错误;B、每生成32g氧气,应转移2NA个电子,错误;C、分子数为NA的气体,其物质的量为1mol,在标准状况下的体积为22.4L,CO、C2H4的摩尔质量均为28g/mol,所以其质量为28g,正确;D、4.6gNa与适量氧气完全反应的混合物中,其阴离子为O2-和O22-应与阳离子Na+数目的1/2相同均等于0.1NA,错误,答案选C。
考点:考查对化学式的理解,氧化还原反应的认识及阿伏伽德罗定律的应用

练习册系列答案
相关题目
某固体A在一定条件下加热分解,产物全是气体,A的分解反应为:2A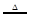 B+2C+2D,现测得分解产生的混合气体对氢气的相对密度为d,则A的相对分子质量为
B+2C+2D,现测得分解产生的混合气体对氢气的相对密度为d,则A的相对分子质量为
| A.2d | B.10d | C.5d | D.0.8d |
下列有关化学用语表示正确的是( )
| A.漂白粉有效成分的化学式:CaClO |
B.Na+的结构示意图: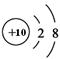 |
C.原子核内有10个中子的氧原子: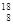 O O |
| D.NaHCO3在水溶液中的电离方程式:NaHCO3=Na++H++CO32— |
室温时,甲、乙两同学在实验室配制氯化钠溶液。甲同学配制5%的NaCl溶液100 g,乙同学配制0.5 mol/L的NaCl溶液100 mL(20 ℃时,氯化钠的溶解度为36 g)。下列说法正确的是( )
| A.两同学所需溶质的质量相同 |
| B.两同学所需实验仪器种类相同 |
| C.两同学所配溶液均为不饱和溶液 |
| D.两同学所配溶液的质量相同 |
用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A.常温常压下,18 g H218O含有的原子总数为3NA |
| B.标准状况下,4.2 g CH2=CH2和CH3CH=CH2的混合气体中所含有的碳原子数为0.3NA |
| C.将0.1 mol Cl2通入1 L水中,转移的电子数目为0.1NA |
| D.0.1 mol·L-1Al2(SO4)3溶液中含有的Al3+总数为0.2NA |
设NA代表阿伏加德罗常数的值,下列说法正确的是( )
| A.1 mol甲基(—CH3)中含有电子数为7NA |
| B.25 ℃时,pH=7的NH4Cl和NH3·H2O的混合溶液中,OH-数为10-7NA |
| C.4.6 g乙醇中含有共价键数目为0.8NA |
| D.两份均为2.7 g的铝样品分别与100 mL浓度均为2 mol·L-1的盐酸和氢氧化钠溶液充分反应,转移电子数均为0.3NA |
下列有关化学用语表示正确的是 ( )。
| A.二氧化硅的分子式:SiO2 |
| B.聚乙烯的结构简式:CH2CH2 |
| C.高氯酸钠(NaClO4)中Cl元素的化合价:+6 |
| D.Mg5(Si4O10)2(OH)2·4H2O的氧化物形式:5MgO·8SiO2·5H2O |
如图是某硫酸试剂瓶标签上的部分文字。据此,下列说法正确的是( )
| 硫酸 化学纯(CP)(500 mL) 品名:硫酸 化学式:H2SO4 相对分子质量:98 密度:1.84 g/cm3 质量分数:98% |
A.该硫酸的物质的量浓度为9.2 mol/L
B.1 mol Zn与足量的该硫酸反应生成2 g氢气
C.该硫酸与等体积水混合所得溶液的物质的量浓度等于9.2 mol/L
D.向50 mL该硫酸溶液中加入足量的铜片,加热充分反应后,被还原的硫酸的物质的量小于0.46 mol
设NA为阿伏加德罗常数的数值,则下列说法中正确的是( )
A.常温下,0.1 mol碳酸钠晶体中含有C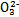 的个数为0.1NA 的个数为0.1NA |
| B.标准状况下22.4 L H2O所含分子数为NA |
| C.1 L 0.5 mol·L-1 CH3COOH溶液中,CH3COO-的个数为0.5NA |
| D.在NO、NO2的混合气体22.4 L中,含有的氮原子数为NA个 |