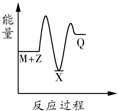
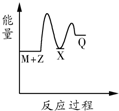
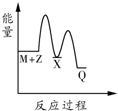
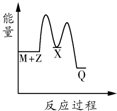
关于化学反应与能量的说法正确的是( )
| A、化学键断裂放出能量 | B、反应物总能量与生成物总能量一定相等 | C、任何化学反应都伴随有能量变化 | D、反应物的总能量高于生成物的总能量时,发生吸热反应 |
最新研究发现,复合氧化物铁酸锰(MnFe2O4)可用于热化学循环分解制氢气:
①MnFe2O4(s)=MnFe2O(4-x)(s)+x/2O2(g);△H1
②MnFe2O(4-x)(s)+xH2O(g)=MnFe2O4(s)+xH2(g);△H2
下列说法错误的是( )
①MnFe2O4(s)=MnFe2O(4-x)(s)+x/2O2(g);△H1
②MnFe2O(4-x)(s)+xH2O(g)=MnFe2O4(s)+xH2(g);△H2
下列说法错误的是( )
| A、反应①中O2是氧化产物,反应②中水是氧化剂 | B、该热化学循环制氢过程简单、无污染,物料可循环使用,安全易分离 | C、若MnFe2O(4-x)(s)中x=0.8,则MnFe2O(4-x)(s)中Fe2+占全部铁元素的百分率为60% | D、若xH2(g)+x/2O2 (g)=xH2O(g);△H3,则△H3=-(△H1+△H2) |
下列说法错误的是( )
| A、化学反应中化学键的断裂和形成是反应过程中有能量变化的本质原因 | ||
| B、常温常压下,用惰性电极电解500mL饱和氯化钠溶液时,若溶液的pH变为13时,则可产生的气体体积为2.24L | ||
| C、NaHSO4溶液与Ba(OH)2溶液反应至中性的离子方程式为:2H++SO42-+Ba2++2OH-═BaSO4↓+2H2O | ||
D、在保持常温下,向醋酸溶液中不断加入CH3COONa固体至溶液的PH=7,则醋酸的电离度减小,
|
下列关于化学变化的叙述错误的是( )
| A、化学变化一定伴随能量变化 | B、化学变化一定有化学键的断裂和生成 | C、化学变化一定伴随物质的状态变化 | D、化学变化一定有新物质生成 |
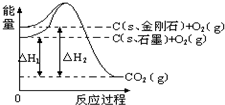 图中△H1=-393.5kJ?mol-1,△H2=-395.4kJ?mol-1,有关说法正确的是( )
图中△H1=-393.5kJ?mol-1,△H2=-395.4kJ?mol-1,有关说法正确的是( )| A、金刚石比石墨稳定性强 | B、石墨变为金刚石是物理变化 | C、石墨变为金刚石是放热反应 | D、1mol石墨的总键能比1mol金刚石的总键能大1.9kJ |
已知:H2(g)+
O2(g)═H2O(l)△H1=-285.8kJ?mol-1①
H2(g)═H2(l)△H2=-0.92kJ?mol-1②
O2(g)═O2(l)△H3=-6.84kJ?mol-1③
H2O(g)═H2O(l)△H4=-44kJ?mol-1④
下列说法正确的是( )
| 1 |
| 2 |
H2(g)═H2(l)△H2=-0.92kJ?mol-1②
O2(g)═O2(l)△H3=-6.84kJ?mol-1③
H2O(g)═H2O(l)△H4=-44kJ?mol-1④
下列说法正确的是( )
| A、上述四个反应都是吸热反应 | ||
| B、1mol液态H2的能量大于1mol气态H2的能量 | ||
| C、H2的燃烧热(△H)为-285.8kJ?mol-1 | ||
D、火箭中液氢燃烧的热化学方程式为H2(l)+
|
盖斯定律在生产和科学研究中有很重要的意义,有些反应的反应热虽然无法直接测得,但可以用盖斯定律间接求得.已知3.6g碳在6.4g的氧气中燃烧,至反应物耗尽,并放出x kJ热量;已知每摩尔单质碳完全燃烧生成CO2放出热量为y kJ,则1mol C与O2反应生成CO的反应热△H为( )
| A、-y kJ?mol-1 | B、-(10x-y)kJ?mol-1 | C、-(5x-0.5y)kJ?mol-1 | D、+(10x-y)kJ?mol-1 |
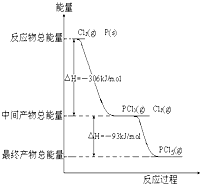 红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g).反应过程和能量关系如图所示(图中的△H表示生成1mol产物的数据).根据图判断,下列叙述正确的是( )
红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g).反应过程和能量关系如图所示(图中的△H表示生成1mol产物的数据).根据图判断,下列叙述正确的是( )| A、P和Cl2分两步反应生成1molPCl5的△H3=399 kJ?mol-1 | ||
| B、P和Cl2一步反应生成1molPCl5的△H4<△H3 | ||
C、P和Cl2反应生成PCl3的热化学方程式为:P(s)+
| ||
| D、PCl5分解成PCl3和Cl2的热化学方程式为:PCl5(g)=PCl3(g)+Cl2(g)△H=93kJ?mol-1 |
在容积不变的密闭容器中加入1mol N2和3mol H2发生反应,下列叙述正确的是( )

| A、该反应的热化学方程式为:N2+3H2?2NH3△H=-92 kJ/mol | B、达到平衡后向容器中通入1mol氦气,平衡不移动 | C、曲线b表示可能使用了催化剂 | D、降低温度和缩小容器体积均可使该反应平衡常数增大 |