题目内容
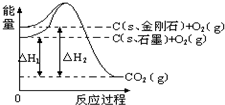 图中△H1=-393.5kJ?mol-1,△H2=-395.4kJ?mol-1,有关说法正确的是( )
图中△H1=-393.5kJ?mol-1,△H2=-395.4kJ?mol-1,有关说法正确的是( )| A、金刚石比石墨稳定性强 | B、石墨变为金刚石是物理变化 | C、石墨变为金刚石是放热反应 | D、1mol石墨的总键能比1mol金刚石的总键能大1.9kJ |
分析:A、图象分析可知金刚石能量高于石墨;
B、石墨和金刚石为碳元素的同素异形体,相互转化为化学变化;
C、图象分析可知石墨变化为金刚石过程是吸热反应;
D、金刚石和石墨燃烧生成二氧化碳气体的焓变,结合焓变=反应物键能总和-生成物键能总和计算;
B、石墨和金刚石为碳元素的同素异形体,相互转化为化学变化;
C、图象分析可知石墨变化为金刚石过程是吸热反应;
D、金刚石和石墨燃烧生成二氧化碳气体的焓变,结合焓变=反应物键能总和-生成物键能总和计算;
解答:解:A、图象分析可知金刚石能量高于石墨,能量越高越活泼,所以石墨稳定,故A错误;
B、石墨和金刚石为碳元素的同素异形体,相互转化为化学变化,故B错误;
C、图象分析可知,石墨的能量低于金刚石,石墨变化为金刚石过程是吸热反应过程,故C错误;
D、金刚石和石墨燃烧生成二氧化碳气体的焓变,结合盖斯定律分析,石墨燃烧焓变△H1=-393.5kJ?mol-1,金刚石燃烧焓变△H2=-395.4kJ?mol-1,1mol石墨的总键能比1mol金刚石的总键能大1.9kJ,故D正确;
故选D.
B、石墨和金刚石为碳元素的同素异形体,相互转化为化学变化,故B错误;
C、图象分析可知,石墨的能量低于金刚石,石墨变化为金刚石过程是吸热反应过程,故C错误;
D、金刚石和石墨燃烧生成二氧化碳气体的焓变,结合盖斯定律分析,石墨燃烧焓变△H1=-393.5kJ?mol-1,金刚石燃烧焓变△H2=-395.4kJ?mol-1,1mol石墨的总键能比1mol金刚石的总键能大1.9kJ,故D正确;
故选D.
点评:本题考查了化学反应能量变化,图象分析判断,焓变与键能大小的分析判断和计算应用,掌握基础是解题关键,题目难度中等.

练习册系列答案
相关题目
 Ni(CO)4(g) 该反应的△H
Ni(CO)4(g) 该反应的△H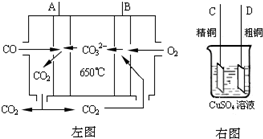
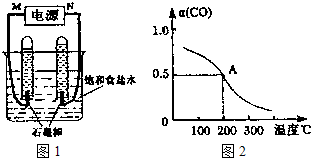
 CH3OH(g);CO的转化率(α)与温度、压强的关系如图所示.
CH3OH(g);CO的转化率(α)与温度、压强的关系如图所示.
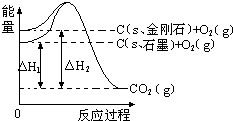 如图所示,△H1=-393.5kJ?mol-1,△H2=-395.4kJ?mol-1,下列说法或表示中,正确的是( )
如图所示,△H1=-393.5kJ?mol-1,△H2=-395.4kJ?mol-1,下列说法或表示中,正确的是( )