题目内容
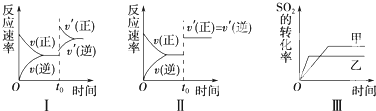
在容积不变的密闭容器中加入1mol N2和3mol H2发生反应,下列叙述正确的是( )

| A、该反应的热化学方程式为:N2+3H2?2NH3△H=-92 kJ/mol | B、达到平衡后向容器中通入1mol氦气,平衡不移动 | C、曲线b表示可能使用了催化剂 | D、降低温度和缩小容器体积均可使该反应平衡常数增大 |
分析:A、热化学方程式需要标注物质聚集状态;
B、恒温恒容容器中加入惰气,体系总压增大,分压不变,平衡不动;
C、催化剂降低反应活化能,增大反应速率,不改变化学平衡,焓变不变;
D、平衡常数随温度变化;
B、恒温恒容容器中加入惰气,体系总压增大,分压不变,平衡不动;
C、催化剂降低反应活化能,增大反应速率,不改变化学平衡,焓变不变;
D、平衡常数随温度变化;
解答:解:A、该反应的热化学方程式为:N2(g)+3H2(g)?2NH3(g) △H=508KJ/mol-600KJ/mol=-92 kJ/mol,故A错误;
B、恒温恒容容器中加入惰气,体系总压增大,分压不变,平衡不动,达到平衡后向容器中通入1mol氦气,平衡不移动,故B正确;
C、催化剂降低反应活化能,增大反应速率,不改变化学平衡,焓变不变,曲线b表示可能使用了催化剂,故C正确;
D、降低温度和缩小容器体积均可使化学平衡发生移动,平衡常数随温度变化,该反应平衡常数不变,故D错误;
故选BC.
B、恒温恒容容器中加入惰气,体系总压增大,分压不变,平衡不动,达到平衡后向容器中通入1mol氦气,平衡不移动,故B正确;
C、催化剂降低反应活化能,增大反应速率,不改变化学平衡,焓变不变,曲线b表示可能使用了催化剂,故C正确;
D、降低温度和缩小容器体积均可使化学平衡发生移动,平衡常数随温度变化,该反应平衡常数不变,故D错误;
故选BC.
点评:本题考查了化学反应焓变,平衡影响因素的分析判断,平衡常数随温度变化,掌握基础和平衡移动原理的应用是关键,题目难度中等.

练习册系列答案
相关题目
在容积不变的密闭容器中进行反应:2SO2( g )+O2( g)?2SO3(g );△H<O.如图表示当其它条件不变时,改变某一条件对上述反应的影响,其中分析正确的是( )
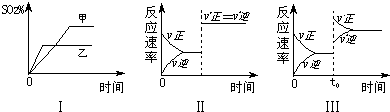

| A、图Ⅰ表示温度对化学平衡的影响,且甲的温度较高 | B、图Ⅱ表示t0时刻使用催化剂对反应速率的影响 | C、图Ⅱ表示t0时刻通入氦气对反应速率的影响 | D、图Ⅲ表示t0时刻增大O2的浓度对反应速率的影响 |