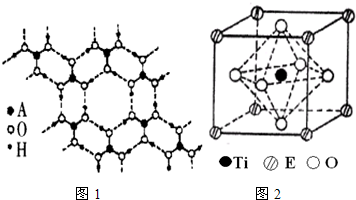
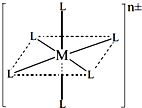
原子数相同、电子总数相同的分子,互称为等电子体.
Ⅰ.已知A、B、C、D和E五种分子所含原子的数目依次为1、2、3、6和6,且都含有18个电子,又知B、C和D是由两种元素的原子组成,且D分子中两种原子个数比为1:2.
请回答:
(1)组成A分子的原子的元素符号是 ;已知E是有毒的有机物,E的熔、沸点比CH4的熔、沸点高,其主要原因是 .
(2)C的立体结构呈 形,该分子属于 分子(填“极性”或“非极性”);
(3)火箭中可充入四氧化二氮和D作为燃料反应生成氮气和水,该反应的化学方程式为 .(不需要写反应条件)
Ⅱ.CO与N2互为等电子体.
(4)CO的总键能大于N2的总键能,但CO比N2容易参加化学反应.
根据下表数据,说明CO比N2活泼的原因是 .
(5)它们的分子中都包含 个σ键, 个π键.
(6)Fe、Co、Ni等金属能与CO反应的原因与这些金属原子的电子层结构有关.
Ni原子的价电子排布式为 .Fe(CO)5常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断Fe(CO)5晶体属于 (填晶体类型);Fe(CO)5是配合物,配体是 .
Ⅰ.已知A、B、C、D和E五种分子所含原子的数目依次为1、2、3、6和6,且都含有18个电子,又知B、C和D是由两种元素的原子组成,且D分子中两种原子个数比为1:2.
请回答:
(1)组成A分子的原子的元素符号是
(2)C的立体结构呈
(3)火箭中可充入四氧化二氮和D作为燃料反应生成氮气和水,该反应的化学方程式为
Ⅱ.CO与N2互为等电子体.
(4)CO的总键能大于N2的总键能,但CO比N2容易参加化学反应.
根据下表数据,说明CO比N2活泼的原因是
| A-B | A=B | A≡B | ||
| CO | 键能(kJ/mol) | 357.7 | 798.9 | 1071.9 |
| 键能差值(kJ/mol) | 441.2 273 | |||
| N2 | 键能(kJ/mol) | 154.8 | 418.4 | 941.7 |
| 键能差值(kJ/mol) | 263.6 523.3 | |||
(6)Fe、Co、Ni等金属能与CO反应的原因与这些金属原子的电子层结构有关.
Ni原子的价电子排布式为
下列是A、B、C、D、E五中元素的某些性质:
(1)元素A是形成有机物的主要元素,下列分子中含有sp和sp3 杂化方式的是
A.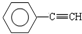 B.CH4 C.CH2=CHCH3D.CH3CH2C≡CH E.CH3CH3
B.CH4 C.CH2=CHCH3D.CH3CH2C≡CH E.CH3CH3
(2)用氢键表示式写出E的氢化物水溶液中存在的所有氢键 .
(3)相同条件下,AD2与BD2分子两者在水中的溶解度较大的是 (写分子式),理由是 ;
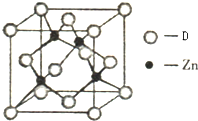
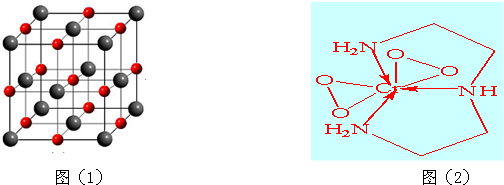
(4)如图表示某种元素D与锌形成的化合物晶胞,其中Zn和D通过共价键结合,该化合物的化学式为 ;该化合物的晶体熔点比干冰高得多,原因是 .
0 22001 22009 22015 22019 22025 22027 22031 22037 22039 22045 22051 22055 22057 22061 22067 22069 22075 22079 22081 22085 22087 22091 22093 22095 22096 22097 22099 22100 22101 22103 22105 22109 22111 22115 22117 22121 22127 22129 22135 22139 22141 22145 22151 22157 22159 22165 22169 22171 22177 22181 22187 22195 203614
| A | B | C | D | E | |
| 化合价 | -4 | -2 | -1 | -2 | -1 |
| 电负性 | 2.55 | 2.58 | 3.16 | 3.44 | 3.98 |
A.
 B.CH4 C.CH2=CHCH3D.CH3CH2C≡CH E.CH3CH3
B.CH4 C.CH2=CHCH3D.CH3CH2C≡CH E.CH3CH3(2)用氢键表示式写出E的氢化物水溶液中存在的所有氢键
(3)相同条件下,AD2与BD2分子两者在水中的溶解度较大的是
(4)如图表示某种元素D与锌形成的化合物晶胞,其中Zn和D通过共价键结合,该化合物的化学式为

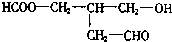 ,若使X通过化学变化失去光学活性,
,若使X通过化学变化失去光学活性,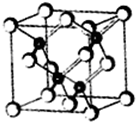 铟、镓与氮、磷、硫、砷等元素形成的化合物是制备LED晶片的主要原料,材质基本以AlGaInP(磷化铝镓铟)、InGaN(氮化铟镓)为主.
铟、镓与氮、磷、硫、砷等元素形成的化合物是制备LED晶片的主要原料,材质基本以AlGaInP(磷化铝镓铟)、InGaN(氮化铟镓)为主.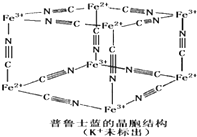 (1)铁及铁的化合物在生产、生活中有着重要的用途.
(1)铁及铁的化合物在生产、生活中有着重要的用途.