镍电池广泛应用于混合动力汽车系统,电极材料由Ni(OH)2、碳粉、氧化铁等涂覆在铝箔上制成.由于电池使用后电极材料对环境有危害,某兴趣小组对该电池电极材料进行资源回收研究,设计实验流程如下:
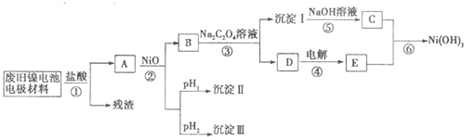
已知:①NiCl2易溶于水,Fe3+不能氧化Ni2+
②某温度下一些金属氢氧化物的Kap及沉淀析出的理论pH如下表所示:
回答下列问题:
(1)根据上表数据判断步骤②依次析出沉淀Ⅱ 和沉淀Ⅲ (填化学式),则pH1 pH2(填填“>”、“=”或“<”),控制两种沉淀析出可利用 .
A.pH试纸B.石蕊指示剂 C.pH计
(2)已知溶解度:NiC2O4>NiC2O4?H2O>NiC2O4?2H2O,则③的化学方程式是 .第③步反应后,过滤沉淀时需要的玻璃仪器有 .若过滤时发现滤液中有少量浑浊,从实验操作的角度给出两种可能的原因 、 .
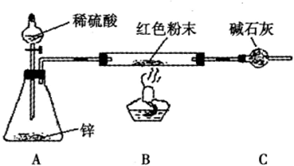
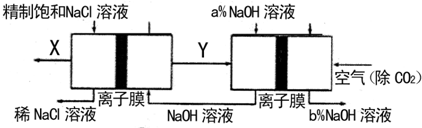
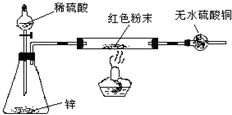
(3)④中阳极反应产生的气体E为 ,验证该气体的试剂为 .
(4)试写出⑥的离子方程式 .

已知:①NiCl2易溶于水,Fe3+不能氧化Ni2+
②某温度下一些金属氢氧化物的Kap及沉淀析出的理论pH如下表所示:
| M(OH)n | Kap | pH | |
| 开始沉淀 | 沉淀完全 | ||
| Al(OH)3 | 1.9×10-23 | 3.43 | 4.19 |
| Fe(OH)3 | 3.8×10-38 | 2.53 | 2.94 |
| Ni(OH)2 | 1.6×10-14 | 7.60 | 9.75 |
(1)根据上表数据判断步骤②依次析出沉淀Ⅱ
A.pH试纸B.石蕊指示剂 C.pH计
(2)已知溶解度:NiC2O4>NiC2O4?H2O>NiC2O4?2H2O,则③的化学方程式是
(3)④中阳极反应产生的气体E为
(4)试写出⑥的离子方程式
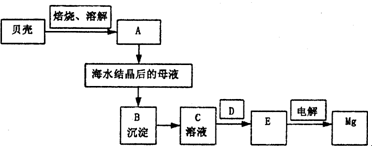
金属镁和镁合金在航空、汽车制造和电子工业等领域具有广泛的用途,金属镁的冶炼有多种方法,其中之一为皮江法.该方法是以白云石(CaCO3?MgCO3)为原料,经高温煅烧生成氧化物(CaO?MgO),氧化物在还原炉中经1200℃真空条件下用硅铁还原生成镁蒸汽(铁在反应前后化合价不变),镁蒸汽经冷凝器冷聚为粗镁,粗镁再经精炼、铸锭得到成品金属镁.反应工艺流程如图1:
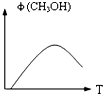
(1)在冶炼过程中反应温度对生成金属镁的影响如图2,从图中分析,还原反应的反应热△H 0(填“<”“>”“=”)理由是 .
(2)还原炉中需要在1200℃真空条件下反应,反应达到平衡时的温度与压强的关系如下
真空条件对制备金属镁来讲,可以达到的目的是:① ②
(3)含镁矿物常见的有菱镁矿(MgCO3)、白云石和光卤石(KCl?MgCl2?6H2O),其中KCl?MgCl2?6H2O属于 .
A.复盐 B.混合物 C.配合物
(4)写出煅烧白云石的反应化学方程式 .
0 21386 21394 21400 21404 21410 21412 21416 21422 21424 21430 21436 21440 21442 21446 21452 21454 21460 21464 21466 21470 21472 21476 21478 21480 21481 21482 21484 21485 21486 21488 21490 21494 21496 21500 21502 21506 21512 21514 21520 21524 21526 21530 21536 21542 21544 21550 21554 21556 21562 21566 21572 21580 203614

(1)在冶炼过程中反应温度对生成金属镁的影响如图2,从图中分析,还原反应的反应热△H
(2)还原炉中需要在1200℃真空条件下反应,反应达到平衡时的温度与压强的关系如下
| 剩余压强mmHg | 760 | 10 | 1 | 0.1 |
| 平衡时的温度℃ | 2370 | 1700 | 1430 | 1235 |
(3)含镁矿物常见的有菱镁矿(MgCO3)、白云石和光卤石(KCl?MgCl2?6H2O),其中KCl?MgCl2?6H2O属于
A.复盐 B.混合物 C.配合物
(4)写出煅烧白云石的反应化学方程式
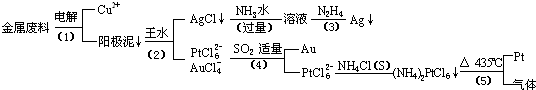
 .
.