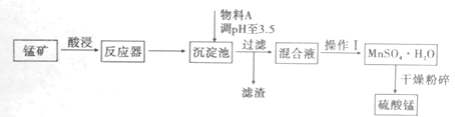
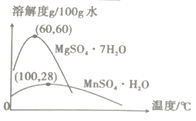
【题目】兰尼镍是一种带有多孔结构的细小晶粒组成的镍铝合金,被广泛用作有机物的氢化反应的催化剂。以红土镍矿(主要成分为NiS、FeS和SiO2等)为原料制备兰尼镍的工艺流程如下图所示:
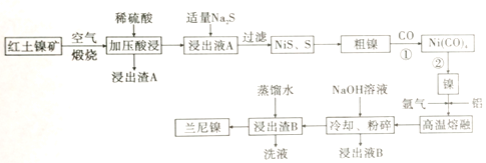
(1)煅烧时生成的主要气体产物是________ ,浸出渣A的主要成分是________。
(2)红土镍矿煅烧后生成的Ni2O3有强氧化性,加压酸浸时有无色无味的气体产生且有NiSO4生成,则该反应中氧化产物与还原产物的物质的量之比为________。
(3)向浸出液A中加入适量Na2S,发生氧化还原反应的离子方程式为________。
(4)若Na2S过量,则过滤出的固体中会混有________;H2S也可代替Na2S使用,但不利之处是________。
(5)已知Ni(CO)4的沸点是42.2℃,Ni(s)+CO(g) ![]() Ni(CO)4(g)的平衡常数与温度关系如下:
Ni(CO)4(g)的平衡常数与温度关系如下:
温度/℃ | 25 | 80 | 230 |
平衡常数 | 5×104 | 2 | 1.9×10-5 |
步骤①、步骤②的最佳温度分别是________、 ________(选填项代号)。
A.25℃ B.30℃ C.50℃ D.80℃ E.230℃
(6)加氢氧化钠的目的是溶解部分铝,形成多孔结构的镍铝合金,已知红土镍矿中NiS质量分数45.5%,取1kg红土镍矿进行制备,熔融时加入270g铝,浸出时消耗800mL 5mol/LNaOH,理论上生成的兰尼镍的化学式为________。