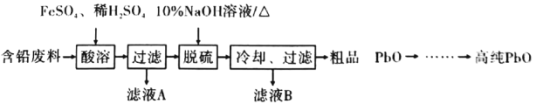
【题目】800℃时,在2L的密闭容器中发生反应:2NO(g)+O2(g)![]() 2NO2,n(NO)随时间的变化如下表所示。
2NO2,n(NO)随时间的变化如下表所示。
时间∕s | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)∕mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(1)从0~3s内,用NO表示的平均反应速率υ(NO)=_____________。
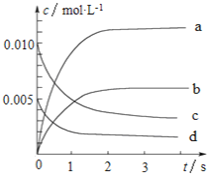
(2)图中表示NO浓度变化的曲线是_______(填字母代号)。
(3)达平衡时NO的转化率为________。
(4)能说明该反应已达到平衡状态的是_________(填序号)。
A.混合气体的颜色保持不变
B.混合气体的密度保持不变
C.υ逆 (NO2)=2υ正 (O2)
D.混合气体的平均相对分子质量保持不变
(5)若升温到850℃,达平衡后n(NO)=n(NO2),则反应向________(填“正反应方向”、“逆反应方向”)移动。
(6)若在一定条件下0.2molNO气体与氧气反应,达平衡时测得放出的热量为akJ,此时NO转化率为80%,则2molNO气体完全反应放出的热量为____________。