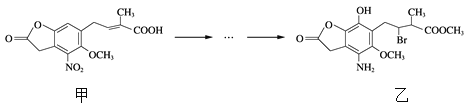
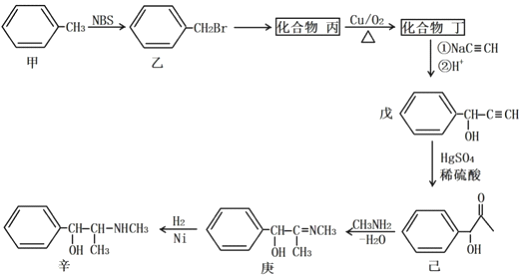
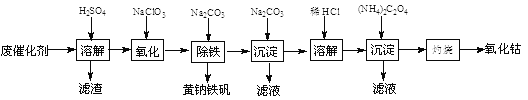
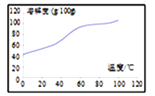
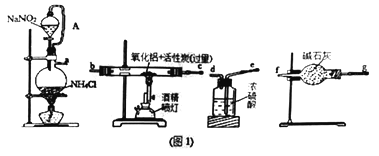
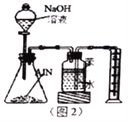
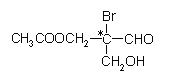0 190811 190819 190825 190829 190835 190837 190841 190847 190849 190855 190861 190865 190867 190871 190877 190879 190885 190889 190891 190895 190897 190901 190903 190905 190906 190907 190909 190910 190911 190913 190915 190919 190921 190925 190927 190931 190937 190939 190945 190949 190951 190955 190961 190967 190969 190975 190979 190981 190987 190991 190997 191005 203614