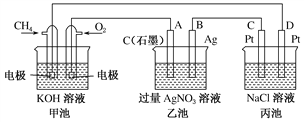
【题目】(Ⅰ)(1)已知在448℃时,反应H2(g)+I2(g)2HI(g)ΔH<0的平衡常数K1为49,则该温度下反应2HI(g)H2(g)+I2(g)的平衡常数K2为______;反应1/2H2(g)+1/2I2(g)HI(g)的平衡常数K3为_______.
(2)在某一密闭容器中发生上述反应,改变反应的某一条件(混合气体的总物质的量不变),造成容器内压强增大,则下列说法中正确的是_____
A.容器内气体的颜色变深,混合气体的密度增大
B.平衡不发生移动
C.I2(g)的转化率增大,H2的平衡浓度变小
D.改变条件前后,速率图象如图所示
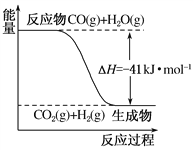
(Ⅱ)在一定体积的密闭容器中,进行如下化学反应:
CO2(g)+H2(g)CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表所示:
t/℃ | 700 | 800 | 830 | 1000 | 1200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
(1)该反应的化学平衡常数表达式为K=______.
(2)该反应为______反应(填“吸热”或“放热”).
(3)能判断该反应达到化学平衡状态的依据是______.
A.容器中压强不变 B.混合气体中c(CO)不变
C.V(H2)正=V(H2O)逆 D.c(CO2)=c(CO)
(4)某温度下,平衡浓度符合下式:c(CO2)c(H2)=c(CO)c(H2O),判断此时温度为______℃.
(5)在800℃时,发生上述反应,某时刻测得容器内各物质的浓度分别为c(CO2)=2mol/L (H2)=1.5mol/L 、 c(CO)=1mol/L 、 c(H2O)=3mol/L,则下一时刻,反应向_________填“正反应”或“逆反应”)方向进行。