5.工业上用软锰矿(主要成分是二氧化锰)制取高锰酸钾和软磁铁氧体材料MnxO4,其流程如下(部分条件和产物省略):

请回答下列问题:
(1)K2MnO4中锰元素的化合价是+6.
(2)写出粉碎矿石和氢氧化钾熔融物中通入空气时,发生主要反应的化学方程式2MnO2+4KOH+O2$\frac{\underline{\;高温\;}}{\;}$2K2MnO4+2H2O.
(3)分析下表数据.工业上采用Ⅲ得到较纯净的高锰酸钾,Ⅲ中包含的操作名称是蒸发结晶、过滤、洗涤、干燥.
(4)上述工业流程中试剂X的最佳物质是(填化学式)Ca(OH)2(或CaO);设计步骤Ⅳ的目的是循环利用二氧化锰、氢氧化钾,提高原料利用率.
(5)通过煅烧MnSO4•H2O可制得软磁铁氧体材料MnxO4.下图是煅烧MnSO4•H2O时温度与剩余固体质量变化的曲线.该曲线中A段所表示物质的化学式是MnSO4;MnxO4中x=3.


请回答下列问题:
(1)K2MnO4中锰元素的化合价是+6.
(2)写出粉碎矿石和氢氧化钾熔融物中通入空气时,发生主要反应的化学方程式2MnO2+4KOH+O2$\frac{\underline{\;高温\;}}{\;}$2K2MnO4+2H2O.
(3)分析下表数据.工业上采用Ⅲ得到较纯净的高锰酸钾,Ⅲ中包含的操作名称是蒸发结晶、过滤、洗涤、干燥.
| 温度/℃ 溶解度/g | 10 | 20 | 30 | 40 | 60 |
| KC2O3 | 107 | 109 | 111 | 114 | 126 |
| KMnO4 | 2.83 | 4.31 | 6.34 | 9.03 | 12.6 |
(5)通过煅烧MnSO4•H2O可制得软磁铁氧体材料MnxO4.下图是煅烧MnSO4•H2O时温度与剩余固体质量变化的曲线.该曲线中A段所表示物质的化学式是MnSO4;MnxO4中x=3.

4.常见金属单质A可发生如图所示转化(部分反应物、产物和反应条件已略去).F是一种温室气体;气体G的水溶液显弱碱性;H是一种具有磁性的黑色氧化物;B、C、D、E四种化合物中含有一种相同的元素.
请回答下列问题:
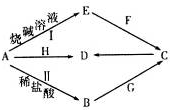
(1)写出F的电子式 ,实验室制取G的化学方程式为Ca(OH)2+2NH4Cl$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2H2O+2NH3↑.
,实验室制取G的化学方程式为Ca(OH)2+2NH4Cl$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2H2O+2NH3↑.
(2)写出反应I的离子方程式2Al+2OH-+2H2O=2AlO2-+3H2↑.该反应中的氧化剂是H2O.
(3)反应I、Ⅱ均有清洁能源H2产生.已知H2的燃烧热为286kJ•mol-1,18g水蒸气变成液态水放出44kJ的热量.其它相关数据如下表:
则表中x为436
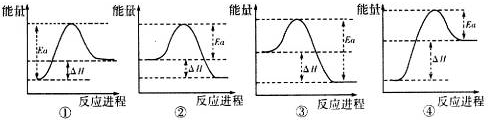
(4)写出A与H反应的化学方程式3Fe3O4+8Al$\frac{\underline{\;高温\;}}{\;}$9Fe+4Al2O3,实验测得该反应的焓变(△H)和活化能(Ea).下列能量关系图合理的是②③(填写序号).
(5)资料显示H可用于除去地下水中的TcO4-(99Tc具有放射性).在酸性条件下,H将TcO4-转化为难溶于水的TcO2,同时得到一种难溶于水的弱碱,该反应的离子方程式为3Fe3O4+TcO4-+13H2O+H+=TcO2+9Fe(OH)3.
请回答下列问题:

(1)写出F的电子式
 ,实验室制取G的化学方程式为Ca(OH)2+2NH4Cl$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2H2O+2NH3↑.
,实验室制取G的化学方程式为Ca(OH)2+2NH4Cl$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2H2O+2NH3↑.(2)写出反应I的离子方程式2Al+2OH-+2H2O=2AlO2-+3H2↑.该反应中的氧化剂是H2O.
(3)反应I、Ⅱ均有清洁能源H2产生.已知H2的燃烧热为286kJ•mol-1,18g水蒸气变成液态水放出44kJ的热量.其它相关数据如下表:
| O=O(g) | H-H(g) | H-O(g) | |
| 键能/kJ•mol-1 | 496 | x | 463 |
(4)写出A与H反应的化学方程式3Fe3O4+8Al$\frac{\underline{\;高温\;}}{\;}$9Fe+4Al2O3,实验测得该反应的焓变(△H)和活化能(Ea).下列能量关系图合理的是②③(填写序号).

(5)资料显示H可用于除去地下水中的TcO4-(99Tc具有放射性).在酸性条件下,H将TcO4-转化为难溶于水的TcO2,同时得到一种难溶于水的弱碱,该反应的离子方程式为3Fe3O4+TcO4-+13H2O+H+=TcO2+9Fe(OH)3.
3.下列描述与图象相对应的是( )


| A. | 图①表示向乙酸溶液中通入氨气至过量的过程中溶液导电性的变化 | |
| B. | 图②表示向1 L l mol•L-1.FeBr2溶液中通入Cl2时Br-物质的量的变化 | |
| C. | 图③表示向Ca(HCO3)2溶液中滴加NaOH溶液时沉淀质量的变化 | |
| D. | 图④表示向一定浓度的Na2CO3溶液中滴加盐酸,生成CO2的物质的量与滴加盐酸物质的量的关系 |
2.LiAlH4、LiH是重要的储氢材料,遇水能剧烈反应放出H2,LiAlH4在125℃分解为LiH、H2和Al.下列说法错误的是( )
| A. | LiH和D2O反应,所得氢气的摩尔质量为4 g•mol-1 | |
| B. | 1 mol LiAlH4在125℃完全分解转移3 mol电子 | |
| C. | LiH与水反应的化学方程式为LiH+H2O═LiOH+H2↑ | |
| D. | LiH中微粒半径r(Li+)<r(H-) |
1.设NA为阿伏加德罗常数的值.下列说法错误的是( )
| A. | 标准状况下,18 g H2O中含有的质子数为10 NA | |
| B. | 标准状况下,2.24 L C12通入水中,反应转移的电子数为0.1 NA | |
| C. | 常温常压下,53.5 g NH4Cl晶体中含有共价键的数目为4 NA | |
| D. | 常温常压下,2 L 0.5 mol•L-1硫酸钾溶液中阴、阳离子总数大于3 NA |
20.下列反应的离子方程式书写正确的是( )
| A. | 氯化铝溶液中加入过量氨水:A13++4NH3•H2O═4NH4++2H2O+A1O2- | |
| B. | 氯化亚铁溶于稀硝酸:3Fe2++4H++NO3-═3Fe3++NO↑+3H2O | |
| C. | NaHCO3溶液和过量的Ba(OH)2溶液混合:2HCO3-+OH-+Ba2+═BaCO3↓+2H2O+CO32- | |
| D. | 用氨水吸收少量二氧化硫:2NH3•H2O+SO2═2NH4++SO32-+H2O |
19.短周期主族元素W、X、Y、Z原子序数依次增大.W原子的最外层电子数是X原子最外层电子数的两倍,质子数比X原子少5个,Y原子的最外层电子数是次外层电子数的一半,Z和W在同一主族.下列说法正确的是( )
| A. | 原子半径:W<X<Y<Z | |
| B. | X、Y、Z单质的熔点:Z<Y<X | |
| C. | 简单气态氢化物的热稳定性:Y<Z<W | |
| D. | Z元素的最高价氧化物对应水化物的分子中存在非极性共价键 |
18.下列叙述正确的是( )
| A. | Cu与过量的S混合加热,最终得到CuS | |
| B. | 将氯气通入冷的消石灰中制漂白粉 | |
| C. | 常温下,将27 g A1投入足量18.4 mol•L-1的硫酸中,产生1.5 mol H2 | |
| D. | 将SO2不断通入Ba(OH)2溶液中,最终得到白色沉淀 |
17.下列实验操作能达到相应目的是( )
| 编号 | 实验操作 | 目的 |
| A | 取4gNaOH固体溶入100mL水中 | 配制4mol•L-1NaOH溶液 |
| B | 向沸水中逐滴加入1~2mLFeCl3饱和溶液,搅拌并继续煮沸出现浑浊 | 制备Fe(OH)3胶体 |
| C | 测定等物质的量浓度的盐酸、硝酸的pH | 比较Cl、N的非金属性强弱 |
| D | 用熔融氧化铝、CCl4做导电性实验 | 验证两者是离子化合物还是共价化合物 |
| A. | A | B. | B | C. | C | D. | D |
16.下列说法正确的是( )
0 173722 173730 173736 173740 173746 173748 173752 173758 173760 173766 173772 173776 173778 173782 173788 173790 173796 173800 173802 173806 173808 173812 173814 173816 173817 173818 173820 173821 173822 173824 173826 173830 173832 173836 173838 173842 173848 173850 173856 173860 173862 173866 173872 173878 173880 173886 173890 173892 173898 173902 173908 173916 203614
| A. | HClO是弱酸,所以NaClO是弱电解质 | |
| B. | SiO2是酸性氧化物,能与NaOH溶液反应生成盐和水 | |
| C. | O3和O2为同种元素组成的单质,所以O3和O2互为同位素 | |
| D. | Na2O和Na2O2组成元素相同,与H2O的反应产物也相同 |