11.酸雨是指pH<5.6的雨、雪等各种形式的大气降水.二氧化硫是形成酸雨的主要因素之一,它主要是由含硫燃料(煤和石油)燃烧和金属冶炼厂释放的二氧化硫气体造成.酸雨的危害极大,减少二氧化硫等污染物的排放,保护环境是非常重要的.某校化学兴趣小组的学生,分成两组对酸雨及空气中二氧化硫的含量进行了测定.
第一组:取刚降到地面的酸雨水样,进行了如下实验:
实验①:将一片红色的玫瑰花瓣浸在一份水样中;
实验②:向雨水试样中滴加氯化钡溶液,有白色浑浊出现;
实验③:每隔一定时间测定其pH,数据如表Ⅰ所示.
表Ⅰ不同时间酸雨的pH
(1)实验①中一段时间后,观察到红色变浅,可能的原因是酸雨中SO2具有漂白作用.
(2)实验②中生成白色浑浊的离子方程式SO42-+Ba2+=BaSO4↓.
(3)分析实验③中pH数据的变化,你认为可能的原因是(用化学方程式表示):SO2+H2O=H2SO3、2H2SO3+O2=2H2SO4.
(4)如果取该雨水和蒸馏水混合,再测pH,结果将变大(填“变大”“变小”或“不变”).
第二组:拟用下列装置定量分析空气中SO2的含量:

(5)该组同学查资料得到的反应原理为:SO2与酸性KMnO4溶液反应的离子方程式:
5SO2+2MnO4-+2H2O=5SO42-+2Mn2++4H+.
该反应的现象是高锰酸钾溶液紫色褪去,SO2在该反应中显还原(填“氧化”或“还原”)性.
(6)该实验中已知的数据有气体流速aL/min、酸性KMnO4溶液的体积bL,其浓度为cmol/L.若从气体通入到紫色恰好褪去,用时5分钟.则此次取样处的空气中二氧化硫含量为$\frac{32bc}{a}$g/L.
第一组:取刚降到地面的酸雨水样,进行了如下实验:
实验①:将一片红色的玫瑰花瓣浸在一份水样中;
实验②:向雨水试样中滴加氯化钡溶液,有白色浑浊出现;
实验③:每隔一定时间测定其pH,数据如表Ⅰ所示.
表Ⅰ不同时间酸雨的pH
| 测定时间/小时钟 | 0 | 1 | 2 | 4 |
| pH | 4.73 | 4.62 | 4.56 | 4.55 |
(2)实验②中生成白色浑浊的离子方程式SO42-+Ba2+=BaSO4↓.
(3)分析实验③中pH数据的变化,你认为可能的原因是(用化学方程式表示):SO2+H2O=H2SO3、2H2SO3+O2=2H2SO4.
(4)如果取该雨水和蒸馏水混合,再测pH,结果将变大(填“变大”“变小”或“不变”).
第二组:拟用下列装置定量分析空气中SO2的含量:

(5)该组同学查资料得到的反应原理为:SO2与酸性KMnO4溶液反应的离子方程式:
5SO2+2MnO4-+2H2O=5SO42-+2Mn2++4H+.
该反应的现象是高锰酸钾溶液紫色褪去,SO2在该反应中显还原(填“氧化”或“还原”)性.
(6)该实验中已知的数据有气体流速aL/min、酸性KMnO4溶液的体积bL,其浓度为cmol/L.若从气体通入到紫色恰好褪去,用时5分钟.则此次取样处的空气中二氧化硫含量为$\frac{32bc}{a}$g/L.
8.现有氧化铁和氧化铜的混合物mg,加入2.5mol/L的硫酸溶液40mL时,恰好完全溶解.若将2mg这种混合物在氢气流中加热并充分反应,冷却后剩余固体的质量为( )
| A. | 0.8g | B. | 1.6mg | C. | (2m-3.2g) | D. | (2m-1.6)g |
6.A、B、C、D是四种短周期元素,它们的原子序数依次增大.其中A、D元素同主族,B、C元素同周期;由A、B、C、D中的两种元素可形成原子个数比为1:1的多种化合物,甲、乙、丙、丁为其中的四种,它们的元素组成如下表所示:
常温下,甲物质为气体,密度略小于空气;乙物质为液体;丙物质和丁物质为固体且都为离子化合物.请填写下列空白:
(1)丙物质的电子式为Na+[:H]-,丁物质中阴离子与阳离子的个数之比为1:2,写出丁与水反应离子方程式2Na2O2+2H2O=4Na++4OH-+O2↑,.
(2)若标准状况下5.6L甲物质完全燃烧放出的热量为QKJ,试写出表示甲物质燃烧热的热化学方程式CO(g)+$\frac{1}{2}$O2(g)=CO2 (g)△H=-4akJ/mol.
(3)B、C两种元素按原子个数比为1:2可形成化合物戊,A、C、D三种元素按原子个数比为1:1:1可形成化合物己,则己与戊按物质的量之比为3:2完全反应后的溶液中各离子浓度的大小关系为c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+).
5.
| 化合物 | 甲 | 乙 | 丙 | 丁 |
| 组成元素 | B、C | A、C | A、D | C、D |
(1)丙物质的电子式为Na+[:H]-,丁物质中阴离子与阳离子的个数之比为1:2,写出丁与水反应离子方程式2Na2O2+2H2O=4Na++4OH-+O2↑,.
(2)若标准状况下5.6L甲物质完全燃烧放出的热量为QKJ,试写出表示甲物质燃烧热的热化学方程式CO(g)+$\frac{1}{2}$O2(g)=CO2 (g)△H=-4akJ/mol.
(3)B、C两种元素按原子个数比为1:2可形成化合物戊,A、C、D三种元素按原子个数比为1:1:1可形成化合物己,则己与戊按物质的量之比为3:2完全反应后的溶液中各离子浓度的大小关系为c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+).
5.
4. X、Y、Z、W四种物质之间有如图所示的转化关系(部分物质未写全),且已知反应热之间的关系符合等式△H=△H1+△H2.则X、Y可能是 ( )
X、Y、Z、W四种物质之间有如图所示的转化关系(部分物质未写全),且已知反应热之间的关系符合等式△H=△H1+△H2.则X、Y可能是 ( )
①C、CO
②AlCl3、Al(OH)3
③Fe、Fe(NO3)2
④Na2CO3、NaHCO3.
0 173387 173395 173401 173405 173411 173413 173417 173423 173425 173431 173437 173441 173443 173447 173453 173455 173461 173465 173467 173471 173473 173477 173479 173481 173482 173483 173485 173486 173487 173489 173491 173495 173497 173501 173503 173507 173513 173515 173521 173525 173527 173531 173537 173543 173545 173551 173555 173557 173563 173567 173573 173581 203614
 X、Y、Z、W四种物质之间有如图所示的转化关系(部分物质未写全),且已知反应热之间的关系符合等式△H=△H1+△H2.则X、Y可能是 ( )
X、Y、Z、W四种物质之间有如图所示的转化关系(部分物质未写全),且已知反应热之间的关系符合等式△H=△H1+△H2.则X、Y可能是 ( ) ①C、CO
②AlCl3、Al(OH)3
③Fe、Fe(NO3)2
④Na2CO3、NaHCO3.
| A. | ①② | B. | ③④ | C. | ①②③ | D. | ①②③④ |

 .
.

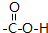 .
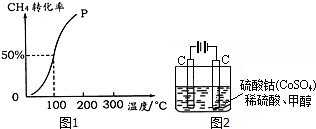
. 如图是一个原电池装置,请按要求填空.
如图是一个原电池装置,请按要求填空.