题目内容
2.实验室用密度为1.84g/mL,质量分数为98%浓硫酸配制500mL 0.2mol/L的稀硫酸溶液,填空并请回答下列问题:(1)配制时,其正确的操作顺序是(字母表示,每个字母只能用一次)BCAFED;
A.用50mL水洗涤烧杯2-3次,洗涤液均注入容量瓶,振荡
B.先在烧杯中加入适量水(约100mL),用量筒准确量取所需的浓硫酸的体积,沿烧杯壁倒入烧杯中,用玻璃棒慢慢搅动,使其混合均匀
C.将已冷却的硫酸沿玻璃棒注入500mL的容量瓶中
D.将容量瓶盖紧,振荡,摇匀
E.改用胶头滴管加水,使溶液凹面恰好与刻度相切
F.继续往容量瓶内小心加水,直到液面接近刻度1-2cm处
(2)若出现如下情况,对所配溶液浓度将有何影响(填“偏高”、“偏低”或“无影响”)?若没有进行A操作偏低;若加蒸馏水时不慎超过了刻度偏低;若定容时俯视刻度线偏高.
(3)若实验过程中出现如下情况如何处理?加蒸馏水时不慎超过了刻度重新配制.
分析 (1)根据配制一定物质的量浓度的溶液的配制步骤排序;
(2)没有A操作,配制的溶液中,溶质的物质的量减小;加水超过了刻度线,配制的溶液体积偏大;俯视刻度线,导致加入的蒸馏水体积偏小;
(3)加蒸馏水时不慎超过了刻度,此次配制失败,需要重新配制.
解答 解:(1)配制溶液的步骤为:计算、量取、稀释、冷却、转移、洗涤、定容,所以正确顺序为:BCAFED,
故答案为:BCAFED;
(2)若没有洗涤烧杯和玻璃棒,配制的溶液中,溶质物质的量减小,溶液浓度偏低;
定容时,加水超过了刻度线,导致溶液的体积偏大,浓度偏低;
若定容时俯视容量瓶刻度线,导致加入的蒸馏水体积偏小,配制的溶液浓度偏高,
故答案为:偏低;偏低;偏高;
(3)配制过程中若加蒸馏水时不慎超过了刻度,则此次配制失败,需要倒入指定的仪器中重新配制,
故答案为:重新配制.
点评 本题考查了配制一定物质的量浓度的溶液方法,题目难度中等,明确配制一定浓度的溶液步骤为解答关键,注意掌握误差分析的方法与技巧,试题培养了学生的灵活应用能力.

练习册系列答案
 科学实验活动册系列答案
科学实验活动册系列答案
相关题目
13.CH3COONa溶液存在水解平衡:CH3COO-+H2O?CH3COOH+OH-,下列说法正确的是( )
| A. | 加入少量NaOH固体,c(CH3COO-)减小 | |
| B. | 加入少量FeCl3固体,c(CH3COO-)减小 | |
| C. | 稀释溶液,溶液的pH增大 | |
| D. | 加入适量醋酸,得到的酸性混合溶液:c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
10.如图所示,将铁棒和石墨棒插入盛有饱和NaCl溶液的U型管中.下列分析正确的是( )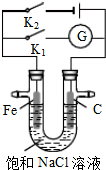

| A. | K1闭合,铁棒上发生的反应为2H++2e-→H2↑ | |
| B. | K1闭合,石墨棒周围溶液pH逐渐降低 | |
| C. | K2闭合,铁棒不会被腐蚀,属于外加电流的阴极保护法 | |
| D. | K2闭合,电路中通过0.4NA个电子时,两极共产生4.48L气体 |
17.分析如图的能量变化示意图,下列热化学方程式正确的是( )


| A. | 2 A(g)+B(g)=2 C(g);△H=a(a>0) | B. | 2 A(g)+B(g)=2 C(g);△H=a(a<0) | ||
| C. | 2A+B=2 C;△H=a(a<0) | D. | 2 C=2 A+B;△H=a(a>0) |
14.下列实验操作、现象和结论均正确的是( )
| 选项 | 实验操作 | 现象 | 结论 |
| A | SO2通入溴水中 | 溶液褪色 | SO2有漂白性 |
| B | 将Fe(NO3)2样品溶于稀H2SO4,滴加KSCN溶液 | 溶液变红 | Fe(NO3)2样品已氧化变质 |
| C | 取等物质的量的两种金属单质X、Y,分别与足量的盐酸反应 | X产生氢气的体积比Y多 | 金属性:X>Y |
| D | 分别向0.1mol•L-1醋酸和饱和硼酸溶液中滴加0.1mol•L-1Na2CO3溶液 | 醋酸中有气泡产生,硼酸中没有气泡产生 | 酸性:醋酸>碳酸>硼酸 |
| A. | A | B. | B | C. | C | D. | D |
12.某同学配制一定物质的量浓度的NaOH溶液,下列情况会造成所配溶液浓度偏低的是( )
| A. | 向容量瓶中加水定容时俯视刻度线 | |
| B. | 称量时所用NaOH已经潮解 | |
| C. | 容量瓶中有蒸馏水 | |
| D. | 溶解后未经冷却就转移到容量瓶进行定容 |
