3.某地区的湖水中可能含有K+、NH4+、Fe3+、Al3+、Mg2+、CO32-、S2O32-、SO42-中的若干种,某研究小组为确定其成分,设计并完成了如下的实验:

已知:Ag2SO4+4S2O32-═2[Ag(S2O3)2]3-+SO42-、Ag2CO3+4S2O32-═2[Ag(S2O3)2]3-+CO32-则下列说法中正确的是( )

已知:Ag2SO4+4S2O32-═2[Ag(S2O3)2]3-+SO42-、Ag2CO3+4S2O32-═2[Ag(S2O3)2]3-+CO32-则下列说法中正确的是( )
| A. | 试样溶液中肯定存在S2O32-、CO32-,可能含有NH4+、Al3+、K+ | |
| B. | 沉淀1的成分肯定为BaSO4和S的混合物 | |
| C. | 将少量气体1通入溶液2中肯定会产生白色沉淀 | |
| D. | 取少量溶液1滴加KSCN溶液,溶液显红色 |
2.已知下列数据,则下列热化学方程式不正确的是( )
| 化学键 | H-H | Cl-Cl | H-Cl |
| 生成(拆开)1mol化学键放出(吸收)的能量 | 436kJ | 243kJ | 431kJ |
| A. | $\frac{1}{2}$H2(g)+$\frac{1}{2}$Cl2(g)═HCl(g)△H=-91.5kJ•mol-1 | |
| B. | $\frac{1}{2}$H2(g)+$\frac{1}{2}$Cl2(g)═HCl(g)△H=+91.5kJ•mol-1 | |
| C. | H2(g)+Cl2(g)═2HCl(g)△H=-183kJ•mol-1 | |
| D. | 2HCl(g)═H2(g)+Cl2(g)△H=+183kJ•mol-1 |
1.二氧化碳与氢气催化合成甲醇,发生的反应为:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)
(1)已知:
计算上述反应的△H=-46kJ•mol-1.
(2)一定条件下,将n(CO2):n(H2)=1:1的混合气充入恒温恒容密闭容器中,下列事实可以说明该反应已达到平衡的是BCEF(填选项字母)
A、容器内气体密度保持不变 B、CO2的体积分数保持不变
C、H2O(g)与CO2(g)的生成速率之比为1:1 D、该反应的平衡常数保持不变
E、混合气体的平均相对分子质量不变 F、容器中压强保持不变
(3)一定条件下,往2L恒容密闭容器中充入1.2molCO2和3.6molH2,在不同催化剂作用下的反应Ⅰ、反应Ⅱ与反应Ⅲ,相同时间内CO2转化率随温度变化的数据如表所示,据表中数据绘制图1:
(T5时,图1中C点转化率为66.67%,即转化了$\frac{2}{3}$)
①催化剂效果最佳的反应是反应Ⅰ(填“反应Ⅰ”、“反应Ⅱ”、“反应Ⅲ”)
②T3的b点v(正)>v(逆).(填“>”“<”“=”)
③T4的a点转化率比T5的c点高原因是该反应为放热反应,温度升高,平衡逆向移动.
④在温度为T5时,该反应的平衡常数K=$\frac{100}{27}$.
⑤在温度为T5时,CH3OH的浓度随时间变化的趋势如图2所示.
当时间到达t1时,将生成的甲醇和水同时除去,并维持该温度,在t2时达到平衡.
请在图2 中画出t1时刻后CH3OH的浓度变化总趋势曲线.

(1)已知:
| 化学键 | H-H | C-O | C=O | H-O | C-H |
| 键能(KJ•mol-1) | 436 | 326 | 803 | 464 | 414 |
(2)一定条件下,将n(CO2):n(H2)=1:1的混合气充入恒温恒容密闭容器中,下列事实可以说明该反应已达到平衡的是BCEF(填选项字母)
A、容器内气体密度保持不变 B、CO2的体积分数保持不变
C、H2O(g)与CO2(g)的生成速率之比为1:1 D、该反应的平衡常数保持不变
E、混合气体的平均相对分子质量不变 F、容器中压强保持不变
(3)一定条件下,往2L恒容密闭容器中充入1.2molCO2和3.6molH2,在不同催化剂作用下的反应Ⅰ、反应Ⅱ与反应Ⅲ,相同时间内CO2转化率随温度变化的数据如表所示,据表中数据绘制图1:
| 相同时间内CO2转化率 | T1 | T2 | T3 | T4 | T5 |
| 反应Ⅰ | 65% | 77% | 80% | 80% | 66.67% |
| 反应Ⅱ | 56% | 67% | 76% | 80% | 66.67% |
| 反应Ⅲ | 48% | 62% | 72% | 80% | 66.67% |
①催化剂效果最佳的反应是反应Ⅰ(填“反应Ⅰ”、“反应Ⅱ”、“反应Ⅲ”)
②T3的b点v(正)>v(逆).(填“>”“<”“=”)
③T4的a点转化率比T5的c点高原因是该反应为放热反应,温度升高,平衡逆向移动.
④在温度为T5时,该反应的平衡常数K=$\frac{100}{27}$.
⑤在温度为T5时,CH3OH的浓度随时间变化的趋势如图2所示.
当时间到达t1时,将生成的甲醇和水同时除去,并维持该温度,在t2时达到平衡.
请在图2 中画出t1时刻后CH3OH的浓度变化总趋势曲线.

1.下列说法不正确的是( )
| A. | 新制的氯水滴到蓝色的石蕊试纸上,试纸由蓝色变红色,最后变无色 | |
| B. | 变色镜遇强光颜色变深主要是由于卤化银见光分解而造成的 | |
| C. | 用有机溶剂就可以从碘水中提取碘单质 | |
| D. | C1-、Br-、I-的还原性随着核电荷数的增大而增强 |
20.一定温度下,mg下列物质在足量的氧气中充分燃烧后,产物与足量的过氧化钠充分反应,过氧化钠增加了mg,不符合此要求的物质是:( )
0 173285 173293 173299 173303 173309 173311 173315 173321 173323 173329 173335 173339 173341 173345 173351 173353 173359 173363 173365 173369 173371 173375 173377 173379 173380 173381 173383 173384 173385 173387 173389 173393 173395 173399 173401 173405 173411 173413 173419 173423 173425 173429 173435 173441 173443 173449 173453 173455 173461 173465 173471 173479 203614
| A. | H2 | B. | CO | C. | H2和CO的混合物 | D. | CH4 |
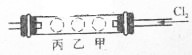 如图所示,有一个硬质玻璃管两端郡装有带导管的单孔塞,在试管中的右、中、左三个部位,分别放入浸有KI淀粉溶液的甲球、浸有NaI浓溶液的乙球和浸有KBr浓溶液的丙球.实验时,从右端缓慢通人C12,同时在乙处微微加热,并将热源从乙向丙处慢慢移动,观察到的现象是:
如图所示,有一个硬质玻璃管两端郡装有带导管的单孔塞,在试管中的右、中、左三个部位,分别放入浸有KI淀粉溶液的甲球、浸有NaI浓溶液的乙球和浸有KBr浓溶液的丙球.实验时,从右端缓慢通人C12,同时在乙处微微加热,并将热源从乙向丙处慢慢移动,观察到的现象是: