17.在一定温度下的定容密闭容器中,下列条件不能表明2A(s)?C(g)+D(g)已达到平衡状态的是( )
| A. | 混合气体的压强不再改变 | |
| B. | 气体C在混合气体中所占的物质的量分数不再改变 | |
| C. | 混合气体的密度不再改变 | |
| D. | 单位时间内消耗n mol C的同时消耗2n mol A |
15.化学概念间存在如图三种关系下列说法中正确的是:( )


| A. | 化合反应与氧化反应属于包含关系 | |
| B. | 吸热反应与放热反应属于交叉关系 | |
| C. | 复分解反应与中和反应属于包含关系 | |
| D. | 含氧化合物与氧化物属于并列关系 |
14.运用相关化学知识进行判断,下列结论错误的是( )
| A. | 某吸热反应能自发进行,因此该反应是熵增反应 | |
| B. | 增大浓度或使用催化剂均能增大活化分子百分数,增大化学反应速率 | |
| C. | 可燃冰主要是甲烷与水在低温高压下形成的水合物晶体,因此可存在于海底 | |
| D. | 铬的价电子电子排布式为3d54s1而不是3d44s2是因为半满稳定 |
13.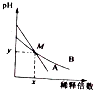 室温下,pH相差1的两种一元碱溶液A和B,分别加水稀释时,溶液的pH变化如图所示,下列说法正确的是( )
室温下,pH相差1的两种一元碱溶液A和B,分别加水稀释时,溶液的pH变化如图所示,下列说法正确的是( )
 室温下,pH相差1的两种一元碱溶液A和B,分别加水稀释时,溶液的pH变化如图所示,下列说法正确的是( )
室温下,pH相差1的两种一元碱溶液A和B,分别加水稀释时,溶液的pH变化如图所示,下列说法正确的是( )| A. | 稀释前,c(A)=10c(B) | |
| B. | 在M点,A、B两种碱溶液中阳离子的物质的量浓度相等 | |
| C. | 稀释前,A溶液中由水电离出的OH-的浓度大于10-7mol/L | |
| D. | 由图可知,A为强碱,B为弱碱 |
12.氮化硅(Si3O4)是一种新型陶瓷材料,它可由石英与焦炭在高温的氮气流中,通过以下反应制得:3SiO2+6C+2N2?Si3N4+6CO.下列叙述不正确的是( )
| A. | 若已知上述反应为放热反应,升高温度,其平衡常数减小 | |
| B. | 上述反应中每生成1molSi3N4,转移12mol电子 | |
| C. | 在氮化硅的合成反应中,N2是氧化剂,SiO2是还原剂 | |
| D. | 若使压强增大,上述平衡向逆反应方向移动 |
11.下列关于原子结构、元素性质的说法正确的是( )
| A. | 元素的电负性:Na>P>Cl | |
| B. | 某元素(R)气态基态原子的逐级电离能分别为738、1451、7733、10540、13630,当它与氯气反应时可能生成的阳离子是R2+ | |
| C. | 具有下列电子排布式的原子中,①1s22s22p63s23p2,②1s22s22p3,③1s22s22p2,④1s22s22p63s23p4,原子半径最大的是④ | |
| D. | ⅦA族元素的阴离子还原性越强,其最高价氧化物对应水化物的酸性就越强 |
10.下列化学用语表示不正确的是( )
| A. | 羟基的电子式: | B. | 石炭酸的结构简式:C6H5OH | ||
| C. | 乙醛的分子式:C2H4O | D. | 酚醛树脂的结构简式为 |
9.25℃,有c(CH3COOH)+c(CH3COO-)=0.1mol•L-1的一组醋酸和醋酸钠混合溶液,溶液中c(CH3COOH)、c(CH3COO-)与pH值的关系如图所示.下列有关离子浓度关系叙述正确的是( )
0 171253 171261 171267 171271 171277 171279 171283 171289 171291 171297 171303 171307 171309 171313 171319 171321 171327 171331 171333 171337 171339 171343 171345 171347 171348 171349 171351 171352 171353 171355 171357 171361 171363 171367 171369 171373 171379 171381 171387 171391 171393 171397 171403 171409 171411 171417 171421 171423 171429 171433 171439 171447 203614

| A. | pH=5.5溶液中:c(CH3COOH)>c(CH3COO-)>c(H+)>c(OH-) | |
| B. | W点表示溶液中:c(Na+)=c(CH3COO-)+c(CH3COOH) | |
| C. | 向W点所表示的1.0L溶液中通入0.05molHCl气体(溶液体积变化可忽略):c(H+)=c(CH3COOH)+c(OH-) | |
| D. | pH=3.5溶液中:c(Na+)+c(H+)-c(OH-)+c(CH3COOH)=0.1mol•L-1 |
 (1)实事证明,能设计成原电池的反应通常是放热反应,下列化学反应在实际中可以设计成原电池的是C
(1)实事证明,能设计成原电池的反应通常是放热反应,下列化学反应在实际中可以设计成原电池的是C
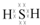 ;其水溶液长期在空气中放置容易变浑浊,该变化体现出:S非金属性比O弱(填“强”或“弱”).用原子结构解释原因:同主族元素最外层电子数相同,从上到下,电子层数增多原子半径增大,得电子能力逐渐减弱.
;其水溶液长期在空气中放置容易变浑浊,该变化体现出:S非金属性比O弱(填“强”或“弱”).用原子结构解释原因:同主族元素最外层电子数相同,从上到下,电子层数增多原子半径增大,得电子能力逐渐减弱.