题目内容
17.在一定温度下的定容密闭容器中,下列条件不能表明2A(s)?C(g)+D(g)已达到平衡状态的是( )| A. | 混合气体的压强不再改变 | |
| B. | 气体C在混合气体中所占的物质的量分数不再改变 | |
| C. | 混合气体的密度不再改变 | |
| D. | 单位时间内消耗n mol C的同时消耗2n mol A |
分析 根据化学平衡状态的特征解答,当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、百分含量不变,以及由此衍生的一些量也不发生变化,解题时要注意,选择判断的物理量,随着反应的进行发生变化,当该物理量由变化到定值时,说明可逆反应到达平衡状态.
解答 解:A、反应前后气体的系数和不等,混合气体的压强不再改变,能表明2A(s)?C(g)+D(g)已达到平衡状态,故A不选;
B、混气体C在混合气体中所占的物质的量分数始终不变,是50%,不能表明2A(s)?C(g)+D(g)已达到平衡状态,故B选;
C、混合气体的密度等于气体质量和体系体积的比值,气体的总物质的量变,体积不变,所以密度变化,当密度不变化了,说明反应达平衡状态,故C不选;
D、单位时间内消耗n mol C的同时消耗2n molA,说明正逆反应速率相等,能表明2A(s)?C(g)+D(g)已达到平衡状态,故D不选;
故选:B.
点评 本题考查了化学平衡状态的判断,难度不大,注意当反应达到平衡状态时,正逆反应速率相等,但不为0.

练习册系列答案
相关题目
4.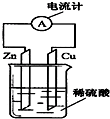 如图是某同学做完Zn-Cu原电池实验后所做的读书卡片记录:实验后的记录:①Cu为负极,发生氧化反应; ②H+向负极移动; ③Cu电极上有气泡产生;④电子流动方向是Zn→导线→Cu.描述合理的是( )
如图是某同学做完Zn-Cu原电池实验后所做的读书卡片记录:实验后的记录:①Cu为负极,发生氧化反应; ②H+向负极移动; ③Cu电极上有气泡产生;④电子流动方向是Zn→导线→Cu.描述合理的是( )
 如图是某同学做完Zn-Cu原电池实验后所做的读书卡片记录:实验后的记录:①Cu为负极,发生氧化反应; ②H+向负极移动; ③Cu电极上有气泡产生;④电子流动方向是Zn→导线→Cu.描述合理的是( )
如图是某同学做完Zn-Cu原电池实验后所做的读书卡片记录:实验后的记录:①Cu为负极,发生氧化反应; ②H+向负极移动; ③Cu电极上有气泡产生;④电子流动方向是Zn→导线→Cu.描述合理的是( )| A. | ①③ | B. | ①④ | C. | ②③ | D. | ③④ |
8.短周期元素在周期表中的位置关系如图所示.
(1)X元素的单质的分子式是He,若X核内中子数与质子数相等,则X的摩尔质量为4g/mol.
(2)Y与氢化合形成的化合物的结构式为H-F,在同主族元素的氢化物分子中,该氢化物分子中共价键键能最大,原因是同主族中F原子半径最小,故H-F键长最短,H-F键最稳定,H-F键能最大.
(3)Z单质的晶体属于分子晶体,Z的氢化物的电子式是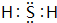 ,该分子中含2个σ键,0个π键(若不含填0).
,该分子中含2个σ键,0个π键(若不含填0).
| X | ||
| Y | ||
| Z |
(2)Y与氢化合形成的化合物的结构式为H-F,在同主族元素的氢化物分子中,该氢化物分子中共价键键能最大,原因是同主族中F原子半径最小,故H-F键长最短,H-F键最稳定,H-F键能最大.
(3)Z单质的晶体属于分子晶体,Z的氢化物的电子式是
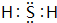 ,该分子中含2个σ键,0个π键(若不含填0).
,该分子中含2个σ键,0个π键(若不含填0).
12.氮化硅(Si3O4)是一种新型陶瓷材料,它可由石英与焦炭在高温的氮气流中,通过以下反应制得:3SiO2+6C+2N2?Si3N4+6CO.下列叙述不正确的是( )
| A. | 若已知上述反应为放热反应,升高温度,其平衡常数减小 | |
| B. | 上述反应中每生成1molSi3N4,转移12mol电子 | |
| C. | 在氮化硅的合成反应中,N2是氧化剂,SiO2是还原剂 | |
| D. | 若使压强增大,上述平衡向逆反应方向移动 |
2.质量数为B的Xn- 阴离子含有a个电子,则中子数为( )
| A. | B-a+n | B. | 2B | C. | B-a-n | D. | 2a |
9.“生活垃圾分类”活动,对提升城市文明和生活质量具有积极的意义.下列四个图为城市生活垃圾分类的标志,则废弃旧电池属于( )
| A. |  可回收垃圾 | B. |  餐厨垃圾 | C. |  有害垃圾 | D. |  其他垃圾 |
6.下列变化中,可由两种单质直接化合生成的是( )
| A. | Fe→FeCl2 | B. | Na→Na2O2 | C. | S→SO3 | D. | N2→NO2 |
7.下列各组中,互为同位素的是( )
| A. | O2和O3 | B. | 3517R和3717R | C. | 2311X和2311X+ | D. | 4018R和4020X |
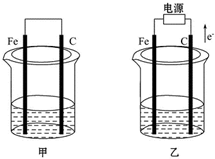 甲、乙两池电极材料都是铁棒与碳棒(如图).请回答下列问题:
甲、乙两池电极材料都是铁棒与碳棒(如图).请回答下列问题: